Elektrisk ledningsevne:Forståelse af ioniske, kovalente, metalliske og polære materialer
* Metallisk: Metaller leder elektricitet meget godt, fordi de har et "hav af elektroner", som kan bevæge sig frit gennem hele strukturen. Disse delokaliserede elektroner kan nemt bære en elektrisk strøm.
* Ionisk: Ioniske forbindelser leder elektricitet, når de opløses i vand eller smeltes. Dette skyldes, at ionerne bliver frie til at bevæge sig og føre strømmen. Men i deres faste tilstand er de dårlige ledere, fordi ionerne er låst fast i et stift gitter.
* Ren kovalent: Rene kovalente forbindelser (som sukker eller vand) leder generelt ikke elektricitet godt, fordi de ikke har fritgående ladede partikler. Elektronerne er tæt bundet i de kovalente bindinger.
* Polar: Polære kovalente molekyler, mens de har en ladningsadskillelse, leder generelt ikke elektricitet godt i deres rene form. Selvom de kan have en vis polariserbarhed, mangler de de frit bevægelige ladninger, der findes i metaller og opløste ioniske forbindelser.
Opsummering: Metaller er de bedste ledere af elektricitet på grund af deres unikke struktur med delokaliserede elektroner.
 Varme artikler
Varme artikler
-
 En simpel mekanisme kunne have været afgørende for livets udviklingEt hold ved det tekniske universitet i München (TUM) har for første gang vist, at faseadskillelse er en yderst effektiv måde at styre udvælgelsen af kemiske byggesten på, giver fordele til visse mol
En simpel mekanisme kunne have været afgørende for livets udviklingEt hold ved det tekniske universitet i München (TUM) har for første gang vist, at faseadskillelse er en yderst effektiv måde at styre udvælgelsen af kemiske byggesten på, giver fordele til visse mol -
 Forskerteam omvendt måde kaliumkanaler fungerer fra bakterier til menneskerGennem deres forskning, Cuello, sammen med D. Marien Cortes, bestemt, hvordan man får hidtil uset viden og kontrol over kaliumkanaler. Kredit:TTUHSC For første gang nogensinde, forskere ved Texas
Forskerteam omvendt måde kaliumkanaler fungerer fra bakterier til menneskerGennem deres forskning, Cuello, sammen med D. Marien Cortes, bestemt, hvordan man får hidtil uset viden og kontrol over kaliumkanaler. Kredit:TTUHSC For første gang nogensinde, forskere ved Texas -
 Lavpris, skalerbar vandspaltning giver næring til fremtidens brintøkonomiMolekylære modeller, der repræsenterer en 2D-heterostruktur lavet af grafen (sexkantet grå baggrundsgitter), og øer på toppen af sekskantede WS2 og MoS, samt en legering af de to. Vand (H2O) molekyl
Lavpris, skalerbar vandspaltning giver næring til fremtidens brintøkonomiMolekylære modeller, der repræsenterer en 2D-heterostruktur lavet af grafen (sexkantet grå baggrundsgitter), og øer på toppen af sekskantede WS2 og MoS, samt en legering af de to. Vand (H2O) molekyl -
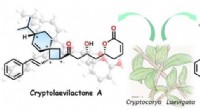 Australsk busk indeholder en ny klasse af organisk forbindelseIsolationer af unikke monoterpen-polyketider med spiro[3, 5]nonan fra C. laevigata . Kredit:Kanazawa University Den botaniske verden kan være et spændende sted for kemikere. Plantearter producer
Australsk busk indeholder en ny klasse af organisk forbindelseIsolationer af unikke monoterpen-polyketider med spiro[3, 5]nonan fra C. laevigata . Kredit:Kanazawa University Den botaniske verden kan være et spændende sted for kemikere. Plantearter producer
- Optisk pumpet laser tættere på at forbedre sensorernes behandlingshastighed
- Hvad er funktionen af solen?
- Hvad er den bedste type sten til fossil dannelse?
- Hvad er anaerob krukke inden for mikrobiologi?
- Når et stort fladt land er løftet, hvad der blev dannet?
- Kvartskrystalsammensætning:Kovalente bindinger forklaret


