Hydrogenfluorid (HF) polaritet:Forståelse af elektronegativitet og bindingsdipoler
* Elektronegativitet: Fluor (F) er det mest elektronegative element, hvilket betyder, at det har en stærk tiltrækning af elektroner. Brint (H) er meget mindre elektronegativt.
* Polær kovalent binding: I et hydrogenfluorid (HF) molekyle trækkes de delte elektroner i bindingen stærkere mod fluoratomet. Dette skaber en delvis negativ ladning (δ-) på fluoren og en delvis positiv ladning (δ+) på brinten.
* Polært molekyle: På grund af denne ujævne ladningsfordeling har HF-molekylet et dipolmoment og betragtes som polært , ikke upolær.
Opsummering: Den ulige deling af elektroner i HF på grund af fluors højere elektronegativitet fører til et polært molekyle, ikke et upolært.
 Varme artikler
Varme artikler
-
 Puster nyt liv i farvesensibiliserede solcellerEt nyt molekylært farvestof forbedrer effektiviteten af solceller. Kredit:Izumi Mindy Takamiya Forskere ved Institute for Integrated Cell-Material Sciences ved Kyoto University har gjort en popu
Puster nyt liv i farvesensibiliserede solcellerEt nyt molekylært farvestof forbedrer effektiviteten af solceller. Kredit:Izumi Mindy Takamiya Forskere ved Institute for Integrated Cell-Material Sciences ved Kyoto University har gjort en popu -
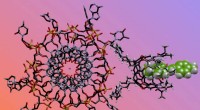 Kemisk næse opsnuser kritiske forskelle i DNA-strukturerIllustration af den kemiske næse, der registrerer en G-quadruplex struktur. Kredit:Richard Hooley/UCR Små ændringer i strukturen af DNA er blevet impliceret i brystkræft og andre sygdomme, men d
Kemisk næse opsnuser kritiske forskelle i DNA-strukturerIllustration af den kemiske næse, der registrerer en G-quadruplex struktur. Kredit:Richard Hooley/UCR Små ændringer i strukturen af DNA er blevet impliceret i brystkræft og andre sygdomme, men d -
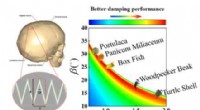 Forholdet mellem sart suturstruktur og dæmpning af biomaterialerFigur 1. De teoretiske modelforudsigelser tyder på, at suturstrukturer fundet i en række naturlige manifestationer har udviklet sig til deres optimale geometrier for at opnå den bedste dæmpningsydelse
Forholdet mellem sart suturstruktur og dæmpning af biomaterialerFigur 1. De teoretiske modelforudsigelser tyder på, at suturstrukturer fundet i en række naturlige manifestationer har udviklet sig til deres optimale geometrier for at opnå den bedste dæmpningsydelse -
 Forskere overvinder barrierer for funktionalisering af bioinspirerede høstmaterialer fra solenergiKredit:Topbillede tilpasset fra Journal of Physical Chemical Letters. Nederste billede, Kara Ng, Naturkemi 2020 Inspireret af naturen, forskere ved City College i New York (CCNY) kan demonstrere
Forskere overvinder barrierer for funktionalisering af bioinspirerede høstmaterialer fra solenergiKredit:Topbillede tilpasset fra Journal of Physical Chemical Letters. Nederste billede, Kara Ng, Naturkemi 2020 Inspireret af naturen, forskere ved City College i New York (CCNY) kan demonstrere
- Hvad er metabolisk stabilitet?
- Oprydning af kulmineforurening i en flod, der er opført på verdensarvslisten
- Hvilken kraft, der forårsager en ændring i bevægelsen af et objekt, kaldes?
- Hvordan er månen i modsætning til Jorden?
- Hvilken form for energi bevæger partikler betyder noget?
- Hvad er lysstråler, der adlyder loven om refleksion, som siger det?


