Forståelse af HCl-molekylær polaritet:Elektronegativitet og bindinger
Her er en opdeling:
* Elektronegativitet: Elektronegativitet er et mål for et atoms evne til at tiltrække elektroner i en kemisk binding. Klor har en højere elektronegativitet end brint.
* Polær kovalent binding: Når to atomer med forskellige elektronegativiteter danner en binding, trækkes de delte elektroner stærkere mod det mere elektronegative atom. Dette skaber en delvis negativ ladning (δ-) på det mere elektronegative atom og en delvis positiv ladning (δ+) på det mindre elektronegative atom.
* HCl-molekyle: I HCl-molekylet bruger de delte elektroner mere tid tættere på kloratomet (på grund af dets højere elektronegativitet). Dette skaber en delvis negativ ladning (δ-) på chloratomet og en delvis positiv ladning (δ+) på hydrogenatomet. Denne ujævne fordeling af ladning resulterer i en polær kovalent binding .
Derfor har HCl-molekylet et dipolmoment , hvilket betyder, at det har en positiv og en negativ ende, hvilket gør det til et polært molekyle .
 Varme artikler
Varme artikler
-
 Cheminformatics tilgange til at skabe nye hårfarverForskere bruger Max Weaver Dye Library til at finde nye, sikrere hårfarveprodukter. Kredit:George Van Den Driessche. At finde den næste generation af sikrere hårfarver kan være lige så simpelt som
Cheminformatics tilgange til at skabe nye hårfarverForskere bruger Max Weaver Dye Library til at finde nye, sikrere hårfarveprodukter. Kredit:George Van Den Driessche. At finde den næste generation af sikrere hårfarver kan være lige så simpelt som -
 En undersøgelse identificerer 17 nøgleforbindelser i vinaromaerKredit:CC0 Public Domain Måske lyder ord som ethylbutanoat og octalactone ukendte for de fleste, der drikker vin. Imidlertid, disse stoffer er nogle af dem, der giver denne populære drik sin egen
En undersøgelse identificerer 17 nøgleforbindelser i vinaromaerKredit:CC0 Public Domain Måske lyder ord som ethylbutanoat og octalactone ukendte for de fleste, der drikker vin. Imidlertid, disse stoffer er nogle af dem, der giver denne populære drik sin egen -
 Chili-formet enhed kunne afsløre, hvor varm den peber erEn chilipeberformet enhed, der indeholder en papirbaseret elektrokemisk sensor, kan tilsluttes en smartphone for at afsløre, hvor meget capsaicin der er i en varm peber. Kredit:Tilpasset fra ACS anve
Chili-formet enhed kunne afsløre, hvor varm den peber erEn chilipeberformet enhed, der indeholder en papirbaseret elektrokemisk sensor, kan tilsluttes en smartphone for at afsløre, hvor meget capsaicin der er i en varm peber. Kredit:Tilpasset fra ACS anve -
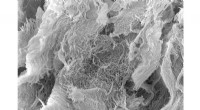 Hydrogel med langsom frigivelse hjælper immunterapi mod kræftEn syntetisk, injicerbar hydrogel udviklet ved Rice University øgede toksiciteten af en ny klasse af kræftbekæmpende immunterapimedicin. Dette scanningselektronmikroskopibillede viser de selvsamlede
Hydrogel med langsom frigivelse hjælper immunterapi mod kræftEn syntetisk, injicerbar hydrogel udviklet ved Rice University øgede toksiciteten af en ny klasse af kræftbekæmpende immunterapimedicin. Dette scanningselektronmikroskopibillede viser de selvsamlede
- Hvilken type fisk er i Choptank River?
- Forskere identificerer afrikansk støv ved at måle isotoper
- Hvilken planet ligger cirka ti gange længere væk fra solen end Jordens sol?
- Hvor mange gram h2o og c3h6 kan der dannes ud fra 6 c3h8o?
- Hvad er bevægelsen af termisk energi fra et sted til et andet, hvad det kaldte?
- Afstand Et objekt rejser pr. Tidsenhed er?


