Hydrogel med langsom frigivelse hjælper immunterapi mod kræft
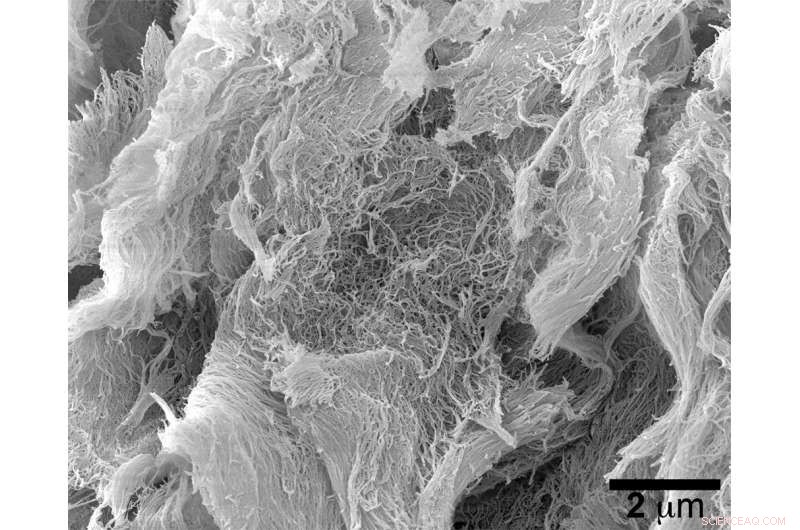
En syntetisk, injicerbar hydrogel udviklet ved Rice University øgede toksiciteten af en ny klasse af kræftbekæmpende immunterapimedicin. Dette scanningselektronmikroskopibillede viser de selvsamlede nanofibre, der udgør hydrogelen. Kredit:Hartgerink Research Group/Rice University
Et immunterapilægemiddel indlejret i en hydrogel med langsom frigivelse, opfundet ved Rice University i samarbejde med University of Texas Health Science Center i Houston (UTHealth), ser ud til at være yderst effektiv til at dræbe kræftceller.
STINGel kombinerer en ny klasse af immunterapi-lægemidler kaldet stimulator af interferon-gen-agonister (STING) med en injicerbar hydrogel, der frigiver lægemidlet i en konstant dosis for at aktivere immunsystemet til at dræbe kræftceller. Det blev udviklet af Rice lab af kemiker og bioingeniør Jeffrey Hartgerink og Rice alun Simon Young, en adjunkt i mund- og kæbekirurgi ved UTHealth.
I kliniske forsøg, immunterapi har vist stærke kræftbekæmpende evner. Forskning har også fundet ud af, at stofferne skylles hurtigt ud af kroppen, og nuværende forsøg kræver flere injektioner.
Den nye forskning, som er detaljeret i Biomaterialer , viste, at slow-release peptidgeler kontinuerligt kunne levere immunterapimedicin til tumorsteder i lange perioder.
Hartgerink er en pioner inden for udvikling af selvsamlende multidomæne peptid (MDP) hydrogeler, som efterligner kroppens ekstracellulære matrix for at fremme væksten af celler og vaskulære systemer til vævsreparation. Hydrogelen injiceres som en væske, bliver halvfast inde i kroppen og nedbrydes langsomt over tid.
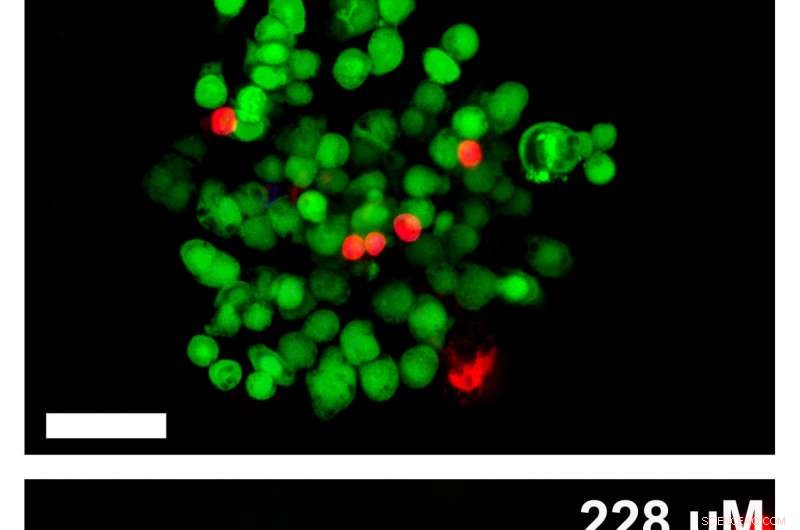
Disse billeder viser, hvordan kræftceller reagerede efter tre dage efter den tidsbestemte frigivelse af immunterapimedicin fra Rice Universitys STINGel. Doser af CDN-immunterapilægemidlet stiger fra top til bund; levende grønne celler viger for døde røde blodlegemer, efterhånden som dosis øges. Skala barer er 50 mikron. Kredit:Hartgerink Research Group/Rice University
Hydrogelen i den nye undersøgelse byder også velkommen til celler, men når angriberne er kræftceller, de er i problemer. Immunterapi-lægemidler kendt som cykliske dinukleotider (CDN'er) venter på dem inde i gelen.
Hartgerink, professor i kemi og bioteknik, sagde, at koncentrationen af CDN i hydrogelen er vigtig.
"Den normale tilgang til CDN levering er simpel injektion, men dette fører til meget hurtig diffusion af lægemidlet i hele kroppen og reducerer dets koncentration på tumorstedet til meget lave niveauer, " sagde han. "Ved at bruge den samme mængde CDN, STINGel-tilgangen tillader, at koncentrationen af CDN nær tumoren forbliver meget højere i lange perioder."
STINGel blev undersøgt både i laboratoriekulturer og in vivo. Til in vivo-delen, seks grupper på 10 gnavere hver blev behandlet med CDN alene, kontrollere kollagener alene eller med CDN, MDP alene eller STINGel (CDN plus MDP). Kun én ud af 10 CDN eller kollagen plus CDN dyr overlevede 105 dage, men seks af 10 dyr behandlet med STINGel overlevede. Disse viste sig også resistente over for yderligere implantation af kræftceller, hvilket betyder, at deres immunsystemer blev trænet til med succes at identificere og ødelægge både den eksisterende kræftsygdom og den fremtidige forekomst af kræften, sagde Hartgerink.
Laboratoriet testede mere almindelige hydrogeler, men fandt ud af, at de ikke var i stand til at give den samme kontrollerede frigivelse og heller ikke gav en yderligere fordel i forhold til CDN-behandling set i kliniske forsøg. "MDP-hydrogelen giver et unikt miljø for frigivelse af CDN, som andre geler bare ikke kan matche, " sagde Hartgerink.
"Den CDN, vi brugte i denne undersøgelse, er i øjeblikket i kliniske forsøg, " sagde han. "Vi mener, at vores STINGel-tilgang har potentialet til betydeligt at udvide omfanget af dette kraftfulde immunterapilægemiddel til et større udvalg af resistente kræftformer."
 Varme artikler
Varme artikler
-
 Forskere udvikler en biologisk nedbrydelig legering til knogleimplantater til frakturer, osteoporose…Lederen af Hybrid Nanostructured Materials Laboratory ved NUST MISIS Alexander Komissarov. Kredit:Maria Brodskaya/NUST MISIS Materialeforskere fra NUST MISIS og University of Western Australia h
Forskere udvikler en biologisk nedbrydelig legering til knogleimplantater til frakturer, osteoporose…Lederen af Hybrid Nanostructured Materials Laboratory ved NUST MISIS Alexander Komissarov. Kredit:Maria Brodskaya/NUST MISIS Materialeforskere fra NUST MISIS og University of Western Australia h -
 Metode til at anvende mikrofluidiske elektrokemiske teknologier til redox-neutrale reaktioner med en…Baggrund og mikrofluidisk redox-neutral elektrokemi (μRN-eChem). Kredit: Videnskab (2020). DOI:10.1126/science.aba3823 Et team af kemikere og ingeniører ved MIT har fundet en ny måde at anvende m
Metode til at anvende mikrofluidiske elektrokemiske teknologier til redox-neutrale reaktioner med en…Baggrund og mikrofluidisk redox-neutral elektrokemi (μRN-eChem). Kredit: Videnskab (2020). DOI:10.1126/science.aba3823 Et team af kemikere og ingeniører ved MIT har fundet en ny måde at anvende m -
 Eksempler på kollektiv ejendomFrostvæske til biler, nyredialyse og brug af sten salt til at fremstille is virker ikke som om de ville have noget til fælles. Men de er alle afhængige af løsningenes koligative egenskaber. Disse e
Eksempler på kollektiv ejendomFrostvæske til biler, nyredialyse og brug af sten salt til at fremstille is virker ikke som om de ville have noget til fælles. Men de er alle afhængige af løsningenes koligative egenskaber. Disse e -
 Hvad er den kemiske MDI?Methylendiphenylisocyanat (MDI) er et kemikalie, der primært bruges til fremstilling af polyurethanskum, der bruges i en række produkter og industrielle anvendelser. Spånplade, en stor del af nybygger
Hvad er den kemiske MDI?Methylendiphenylisocyanat (MDI) er et kemikalie, der primært bruges til fremstilling af polyurethanskum, der bruges i en række produkter og industrielle anvendelser. Spånplade, en stor del af nybygger
- Udvekslingsbias i van der Waals heterostrukturer
- SpaceX udsætter første kommercielle lancering på grund af kraftig vind
- Hvordan små robotter kan forbedre dit helbred fra kroppen
- Børn skal ikke gentage et år i skole på grund af coronavirus. Der er meget bedre muligheder
- Hvad er tilgængeligheden af solenergi?
- Undersøgelse viser, at svingende indkomstusikkerhed kan føre til en nedtur


