Påvisning af alkalinitet i vand efter kaliumreaktion:Metoder og indikatorer
1. Lakmuspapir:
* Procedure: Dyp et stykke rødt lakmuspapir i opløsningen.
* Observation: Det røde lakmuspapir bliver blåt, hvilket indikerer tilstedeværelsen af en base (alkali).
2. pH-papir eller universalindikator:
* Procedure: Dyp et stykke pH-papir eller en dråbe universalindikator i opløsningen.
* Observation: pH-papiret vil vise en farveændring, eller den universelle indikator vil vise en farve svarende til en pH-værdi over 7, hvilket indikerer tilstedeværelsen af en base (alkali).
3. Phenolphtalein-indikator:
* Procedure: Tilsæt et par dråber phenolphtaleinopløsning til vandet.
* Observation: Opløsningen bliver lyserød, hvilket indikerer tilstedeværelsen af en base (alkali).
4. Konduktivitetsmåling:
* Procedure: Brug en ledningsevnemåler til at måle opløsningens elektriske ledningsevne.
* Observation: Ledningsevnen vil være væsentligt højere end rent vand på grund af tilstedeværelsen af opløste ioner (hydroxidioner, kaliumioner) produceret fra reaktionen.
Forklaring:
Reaktionen mellem kalium og vand er meget eksoterm og producerer kaliumhydroxid (KOH), en stærk base. Denne base vil opløses i vand og skabe en opløsning med en høj pH (alkalisk). Metoderne er først og fremmest afhængige af at detektere opløsningens øgede alkalinitet.
Sikkerhed:
* Forsigtig: Kalium reagerer voldsomt med vand og genererer varme. Bær altid passende sikkerhedsudstyr og udfør reaktionen i et stinkskab.
* Rør ikke ved opløsningen med bare hænder.
Vigtig bemærkning: Selvom disse metoder kan påvise tilstedeværelsen af alkali, identificerer de ikke specifikt kaliumhydroxid. Andre alkalier kan også være til stede.
 Varme artikler
Varme artikler
-
 Ny proces fremmer området for kulstofudnyttelseFeng Jiao, lektor i kemisk og biomolekylær teknik ved University of Delaware, er førende inden for kulstofopsamling og -udnyttelse. Kredit:Joy Smoker I et forsøg på at udvikle bæredygtige løsninge
Ny proces fremmer området for kulstofudnyttelseFeng Jiao, lektor i kemisk og biomolekylær teknik ved University of Delaware, er førende inden for kulstofopsamling og -udnyttelse. Kredit:Joy Smoker I et forsøg på at udvikle bæredygtige løsninge -
 Bottom-up syntese af krystallinske 2-D polymererKredit:CC0 Public Domain Forskere ved Center for Advancing Electronics Dresden (cfaed) ved TU Dresden er lykkedes med at syntetisere arklignende 2-D-polymerer ved en bottom-up-proces for første ga
Bottom-up syntese af krystallinske 2-D polymererKredit:CC0 Public Domain Forskere ved Center for Advancing Electronics Dresden (cfaed) ved TU Dresden er lykkedes med at syntetisere arklignende 2-D-polymerer ved en bottom-up-proces for første ga -
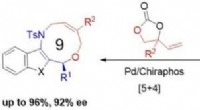 Syntese af mellemstore ringstrukturerede forbindelserFigur viser reaktionsskemaet for kemiske forbindelser med ni- og ti-leddet ringdannelse. Chiraphos og SIPHOX er to kommercielt tilgængelige forbindelser. Kredit:National University of Singapore NU
Syntese af mellemstore ringstrukturerede forbindelserFigur viser reaktionsskemaet for kemiske forbindelser med ni- og ti-leddet ringdannelse. Chiraphos og SIPHOX er to kommercielt tilgængelige forbindelser. Kredit:National University of Singapore NU -
 Konvertering af en empirisk formel til en molekylær formel:en trin-for-trin guideSokRom/iStock/GettyImages Den empiriske formel for en forbindelse udtrykker det enkleste forhold mellem atomer blandt dets bestanddele. Den fortæller dig, hvilke grundstoffer der er til stede og dere
Konvertering af en empirisk formel til en molekylær formel:en trin-for-trin guideSokRom/iStock/GettyImages Den empiriske formel for en forbindelse udtrykker det enkleste forhold mellem atomer blandt dets bestanddele. Den fortæller dig, hvilke grundstoffer der er til stede og dere
- Navngiv to objekter i solsystemet udover måner og planeter?
- Hvilken lov siger, jo større er den masse stærkere gravitationskraftafstand svagere kraft?
- Hvordan er hastighedsmasse og momentum relateret?
- Astronomer undersøger de fysiske egenskaber af galaksen PGC 26218
- Hvad i alverden hjælper med at moderere den samlede temperatur?
- Hvilken del af cellen transporterer materialer i cellen?


