Konvertering af en empirisk formel til en molekylær formel:en trin-for-trin guide
SokRom/iStock/GettyImages
Den empiriske formel for en forbindelse udtrykker det enkleste forhold mellem atomer blandt dets bestanddele. Den fortæller dig, hvilke grundstoffer der er til stede og deres relative proportioner, men ikke det nøjagtige antal atomer i et enkelt molekyle. Molekylformlen afslører på den anden side det præcise antal af hvert atom i et molekyle. Fordi mange forskellige forbindelser deler den samme empiriske formel, kan du kun udlede en molekylær formel, når du også kender forbindelsens molære masse.
TL;DR (for lang; læste ikke)
Når du kender den empiriske formel, skal du beregne dens molære masse. Divider prøvens faktiske masse med denne molære masse for at opnå en heltalsmultiplikator. Multiplicer hvert subscript i den empiriske formel med den multiplikator for at få den molekylære formel.
Sådan bestemmes den empiriske formel
Kemikere bruger almindeligvis en forbrændings- eller titreringsanalyse til at bestemme massen af hvert grundstof i en kendt mængde af forbindelsen. Efter at have målt massen af hvert grundstof skal du dividere med dets atomvægt for at finde antallet af mol. Udtryk disse molforhold som hele tal (eller forenklede fraktioner) for at opnå den empiriske formel, den mest kortfattede repræsentation af forbindelsens sammensætning.
Udledning af den molekylære formel
Følg disse trin:
- Beregn den empiriske masse. Sum produktet af hvert elements atomvægt og dets underskrift i den empiriske formel. Dette giver den molære masse, som den empiriske formel repræsenterer.
- Mål prøvemassen. Vej en ren prøve af forbindelsen (ideelt set i gram).
- Beregn multiplikatoren. Divider prøvemassen med den empiriske masse. Resultatet skal være et heltal (eller meget tæt på et, inden for eksperimentel fejl).
- Skaler den empiriske formel. Multiplicer hvert elements underskrift med heltalsmultiplikatoren for at opnå molekylformlen.
Illustrativt eksempel
Trin 1:Find den empiriske formel
Forbindelsen indeholder 72 g kulstof (C), 12 g hydrogen (H) og 96 g oxygen (O). Beregn antallet af mol:
- C:72g ÷ 12gmol⁻¹ =6mol
- H:12g ÷ 1gmol⁻¹ =12mol
- O:96g ÷ 16gmol⁻¹ =6mol
Divider hver med den mindste værdi (6) for at få det enkleste forhold:1:2:1. Den empiriske formel er CH₂O , det samme som formaldehyd.
Trin 2:Bestem den molekylære formel
Beregn først den empiriske masse:en C (12g) + to H (2g) + en O (16g) =30g. Prøven vejer 180g, så 180g ÷ 30g =6. Multiplicer hver sænket skrift med 6 for at få molekylformlen:C₆H₁₂O₆ , som er glucose. Selvom glucose og formaldehyd deler den samme empiriske formel, udviser de markant forskellige egenskaber - glucose søder, mens formaldehyd er et farligt konserveringsmiddel.
 Varme artikler
Varme artikler
-
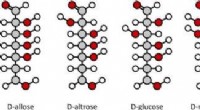 At knække sukkerkoden - hvorfor glykomet er den næste store ting inden for sundhed og medicinKredit:molekuul_be/shutterstock.com Når du tænker på sukker, du tænker sikkert på det søde, hvid, krystallinsk bordsukker, som du bruger til at lave småkager eller søde din kaffe. Men vidste du, a
At knække sukkerkoden - hvorfor glykomet er den næste store ting inden for sundhed og medicinKredit:molekuul_be/shutterstock.com Når du tænker på sukker, du tænker sikkert på det søde, hvid, krystallinsk bordsukker, som du bruger til at lave småkager eller søde din kaffe. Men vidste du, a -
 Hvordan nye materialer øger effektiviteten af direkte ethanolbrændselscellerMaterialet består af Nafion med indlejrede nanopartikler. Kredit:B.Matos/IPEN Ethanol har fem gange højere volumetrisk energitæthed (6,7 kWh/L) end brint (1,3 kWh/L) og kan sikkert bruges i brænds
Hvordan nye materialer øger effektiviteten af direkte ethanolbrændselscellerMaterialet består af Nafion med indlejrede nanopartikler. Kredit:B.Matos/IPEN Ethanol har fem gange højere volumetrisk energitæthed (6,7 kWh/L) end brint (1,3 kWh/L) og kan sikkert bruges i brænds -
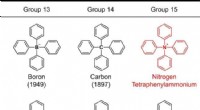 Syntese af tetraphenylammonium:Bekræftelse af eksistensen af fantomionenFigur 1. Strukturer af tetraphenyl-substituerede grundstoffer, der tilhører grupperne 13-15. Tallet i parentes angiver synteseåret. Kredit:Kanazawa University Tetraphenylammonium, med alle fire hyd
Syntese af tetraphenylammonium:Bekræftelse af eksistensen af fantomionenFigur 1. Strukturer af tetraphenyl-substituerede grundstoffer, der tilhører grupperne 13-15. Tallet i parentes angiver synteseåret. Kredit:Kanazawa University Tetraphenylammonium, med alle fire hyd -
 Find forskellen:Støbejern vs. støbt stål forklaretAf Brett Smith Opdateret 24. marts 2022 MSPhotographic/iStock/Getty Images Støbejern og støbestål er begge for det meste lavet af jern og kan derfor næsten ikke skelnes i udseende. De er dog kend
Find forskellen:Støbejern vs. støbt stål forklaretAf Brett Smith Opdateret 24. marts 2022 MSPhotographic/iStock/Getty Images Støbejern og støbestål er begge for det meste lavet af jern og kan derfor næsten ikke skelnes i udseende. De er dog kend
- Hvad laver forskellige slags atomer?
- Hvordan er hydrogenperoxid skadeligt?
- Hvor kontinental skorpe handler om tider tykkere end oceanisk skorpe.?
- Hvordan dannes orografisk nedbør i kystområder?
- Hvad er strukturen af cellreceptorer, som det ses af lysmikroskop?
- Hvilken enhed bruges til opbevaring af den elektriske ladning?


