Ionbindinger forklaret:Hvordan elektroner overføres til dannelse af stærke, ledende forbindelser
SarapulSar38/iStock/GettyImages
Hvad er en ionisk binding?
I kemi opstår en ionbinding, når atomer med markant forskellige elektronegativiteter interagerer. Et atom, typisk et metal, donerer en elektron og bliver til en positivt ladet kation. Recipienten, normalt et ikke-metal, accepterer elektronen og danner en negativt ladet anion. Den elektrostatiske tiltrækning mellem disse modsatte ladninger skaber en robust, polær binding.
Klassiske eksempler inkluderer natriumchlorid (NaCl), det allestedsnærværende bordsalt og svovlsyre (H2SO4), hvor brintatomer overfører elektroner til svovl-oxygen-strukturen. Disse stoffer illustrerer de grundlæggende principper for iondannelse og gittersamling.
Styrken af ioniske vs. kovalente bindinger
Bindingsstyrken kvantificeres ved bindingsdissociationsenergi - den energi, der kræves for at adskille bundne atomer. Ionbindinger udviser generelt højere dissociationsenergier end kovalente bindinger, hvilket afspejler deres stærkere elektrostatiske kræfter. Som følge heraf udviser ioniske forbindelser typisk højere smelte- og kogepunkter og større modstand mod termisk nedbrydning.
Elektrisk ledningsevne og ioniske strukturer
Når ioniske forbindelser opløses i vand eller smelter, bliver deres ioner mobile, hvilket muliggør effektiv elektrisk ledning. Denne egenskab adskiller ioniske materialer fra kovalente stoffer, som mangler frie ladningsbærere. De omfattende tredimensionelle gitter dannet af alternerende kationer og anioner bidrager også til de forhøjede smeltepunkter, der observeres i ioniske faste stoffer.
Skelne ioniske fra kovalente bindinger
Nøgleindikatorer for en ionbinding omfatter:
- Danning mellem et metal og et ikke-metal.
- Høj polaritet og mangel på en defineret molekylær geometri.
- Fast tilstand ved stuetemperatur med høje smelte-/kogepunkter.
- Dissociation til ioner, når de er opløst i vand.
I modsætning hertil involverer kovalente bindinger typisk to ikke-metaller med lignende elektronegativiteter. Disse bindinger deler elektroner, hvilket resulterer i:
- Lavere polaritet og ofte en specifik molekylær form.
- Væskeformig eller gasformig tilstand ved stuetemperatur.
- Begrænset opløselighed i vand, uden ion-dissociation.
At forstå disse skel er afgørende for at forudsige sammensatte adfærd i kemiske reaktioner og industrielle applikationer.
 Varme artikler
Varme artikler
-
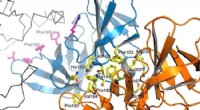 Nyt mål for udvikling af innovative antibiotikaBrasilianske og franske videnskabsmænd viser, at inhibering af interaktionen mellem to nøgleproteiner til cellevægsforlængelse kan være en effektiv strategi til at dræbe bakterier af bacillus-typen. K
Nyt mål for udvikling af innovative antibiotikaBrasilianske og franske videnskabsmænd viser, at inhibering af interaktionen mellem to nøgleproteiner til cellevægsforlængelse kan være en effektiv strategi til at dræbe bakterier af bacillus-typen. K -
 Højtryksforskere opdager lovende materiale til informationsteknologiKredit:CC0 Public Domain Forskere ved University of Bayreuth har opdaget et usædvanligt materiale:Når det køles ned til to grader celsius, dets krystalstruktur og elektroniske egenskaber ændrer si
Højtryksforskere opdager lovende materiale til informationsteknologiKredit:CC0 Public Domain Forskere ved University of Bayreuth har opdaget et usædvanligt materiale:Når det køles ned til to grader celsius, dets krystalstruktur og elektroniske egenskaber ændrer si -
 Paleopharmaceuticals fra baltisk rav kan bekæmpe lægemiddelresistente infektionerBaltisk rav er ikke kun smukt, men også en potentiel kilde til nye antibiotika. Kredit:Connor McDermott I århundreder, mennesker i de baltiske lande har brugt gammelt rav til medicinske formål. Se
Paleopharmaceuticals fra baltisk rav kan bekæmpe lægemiddelresistente infektionerBaltisk rav er ikke kun smukt, men også en potentiel kilde til nye antibiotika. Kredit:Connor McDermott I århundreder, mennesker i de baltiske lande har brugt gammelt rav til medicinske formål. Se -
 Nye farvestoffer registrerer sygdom gennem hjerteslagssignalerUConn Health-forskere udviklede og patenterede spændingsfølsomme farvestoffer, der forårsager celler, væv, eller hele organer til at lyse op som følge af elektriske impulser og tillade denne aktivitet
Nye farvestoffer registrerer sygdom gennem hjerteslagssignalerUConn Health-forskere udviklede og patenterede spændingsfølsomme farvestoffer, der forårsager celler, væv, eller hele organer til at lyse op som følge af elektriske impulser og tillade denne aktivitet
- Sådan verificeres stoffets renhed:Fra visuelle kontroller til avanceret spektroskopi
- Forståelse af opløselighed:Hvorfor nogle stoffer opløses og andre ikke
- Forskere finder enkle, billig måde at øge solcelleeffektiviteten
- Hvordan blev klipper og mineraler brugt i fortiden som værktøjer?
- Undersøgelse viser betydningen af vilde dyr i bekæmpelsen af flåter
- En overmættet opløsning indeholder mindre opløst opløst stof end en mættet ved samme temperatur…


