Forståelse af opløselighed:Hvorfor nogle stoffer opløses og andre ikke
1. Molekylær struktur og intermolekylære kræfter:
* Polaritet: Stoffer med lignende polariteter har en tendens til at opløses i hinanden. "Som opløses ligesom." For eksempel er vand et polært opløsningsmiddel, og det opløser andre polære stoffer som sukker. Ikke-polære stoffer som olie opløses ikke i vand, fordi deres molekylære strukturer ikke interagerer positivt.
* Intermolekylære kræfter: Styrken af tiltrækningerne mellem molekyler påvirker opløseligheden. Stærke intermolekylære kræfter, som brintbinding i vand, kan være svære at overvinde. Stoffer med svagere intermolekylære kræfter er mere tilbøjelige til at opløses.
2. Kemisk reaktivitet:
* Reaktioner: Nogle stoffer reagerer med opløsningsmidlet i stedet for blot at opløses. Dette kan føre til dannelse af nye stoffer, der ikke er opløselige. For eksempel reagerer jern med syrer og danner brintgas og opløselige jernsalte.
3. Fysiske egenskaber:
* Gitterstruktur: Krystallinske faste stoffer har en stiv, organiseret struktur. At bryde disse strukturer fra hinanden kræver en betydelig mængde energi, hvilket er grunden til, at mange faste stoffer ikke opløses let.
* Størrelse og form: Store molekyler eller partikler kan være for omfangsrige til at passe mellem opløsningsmiddelmolekyler, hvilket forhindrer opløsning. Dette er grunden til, at sand ikke opløses i vand.
4. Temperatur og tryk:
* Temperatur: Stigende temperatur øger generelt opløseligheden, da det giver mere energi til at overvinde intermolekylære kræfter. Der er dog undtagelser.
* Tryk: Tryk påvirker primært opløseligheden af gasser. Stigende tryk øger opløseligheden af gasser.
5. Mætning:
* Begrænset opløselighed: Selvom et stof kan opløses, er der en grænse for, hvor meget der kan opløses i en given mængde opløsningsmiddel ved en bestemt temperatur. Når opløsningen når mætning, vil ikke mere opløst stof opløses.
Opsummeret er opløselighed et komplekst fænomen, der påvirkes af flere faktorer. Det handler ikke kun om, hvorvidt et stof kan nedbrydes til mindre partikler, men også hvordan disse partikler interagerer med opløsningsmidlet og det omgivende miljø.
Sidste artikelSaltsyre vs. Svovlsyre:Hovedforskelle forklaret
Næste artikelEksoterm reaktion af lud (NaOH) med vand:Forklaring og kemi
 Varme artikler
Varme artikler
-
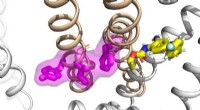 Undersøgelse afslører en ny mekanisme bag epilepsi og lægemiddelmoduleringForskere i Jianmin Cuis laboratorium har set på mekanismerne bag funktionen og dysfunktionen af en gruppe proteiner, samt deres interaktioner med et antiepileptisk lægemiddel, for at udvikle en pote
Undersøgelse afslører en ny mekanisme bag epilepsi og lægemiddelmoduleringForskere i Jianmin Cuis laboratorium har set på mekanismerne bag funktionen og dysfunktionen af en gruppe proteiner, samt deres interaktioner med et antiepileptisk lægemiddel, for at udvikle en pote -
 Udvikling af et fast materiale, der er i stand til langsomt at frigive svovlbrinte og nitrogenoxidFast materiale, der er i stand til at frigive svovlbrinte (H 2 S) og nitrogenoxid (NO), når de udsættes for luft. Kredit:NIMS National Institute for Materials Science har udviklet et fast materi
Udvikling af et fast materiale, der er i stand til langsomt at frigive svovlbrinte og nitrogenoxidFast materiale, der er i stand til at frigive svovlbrinte (H 2 S) og nitrogenoxid (NO), når de udsættes for luft. Kredit:NIMS National Institute for Materials Science har udviklet et fast materi -
 Topologikontrol af humane fibroblastceller monolag ved flydende krystal elastomerEnsartet justering af HDF-celler på LCE med en ensartet nˆLCE=konst. (A) Digital holografisk mikroskopi (DHM) tekstur af LCE-overfladen efter kontakt med det vandige vækstmedium. (B) Fasekontrast-mikr
Topologikontrol af humane fibroblastceller monolag ved flydende krystal elastomerEnsartet justering af HDF-celler på LCE med en ensartet nˆLCE=konst. (A) Digital holografisk mikroskopi (DHM) tekstur af LCE-overfladen efter kontakt med det vandige vækstmedium. (B) Fasekontrast-mikr -
 TNT kan gå på pension efter 116 år på jobbetSprængstofkemiker David Chavez hælder et eksempel på smeltestøbt sprængstof i en kobberform ved Los Alamos National Laboratorys Technical Area 9. Kredit:LANL Forskere ved Los Alamos National Labor
TNT kan gå på pension efter 116 år på jobbetSprængstofkemiker David Chavez hælder et eksempel på smeltestøbt sprængstof i en kobberform ved Los Alamos National Laboratorys Technical Area 9. Kredit:LANL Forskere ved Los Alamos National Labor
- Et omfattende kig på amerikanske standarder for brændstoføkonomi viser store besparelser på bræ…
- Magama der hærder mellem lag af rock?
- Hvordan testosteron regulerer sang på kanariefugle
- Hvad kommer al energi til levende ting i sidste ende fra?
- Kraftfuldt jordskælv vækker folk fra søvn i det sydlige Filippinerne
- Ny forskning afslører hemmelighederne bag fotosyntesen, der kan hjælpe med at udvikle computertekn…


