Forståelse af pH:sure, basiske og neutrale forbindelser forklaret
* Surhed og basicitet er relative begreber: De beskriver en forbindelses tendens til at donere eller acceptere protoner (H+ ioner) i en specifik kontekst (som vand).
* Nogle forbindelser er amfotere: Disse forbindelser kan fungere som både syrer og baser, afhængigt af omstændighederne. Vand i sig selv er et godt eksempel.
* Mange forbindelser er hverken sure eller basiske: De deltager ikke uden videre i protonoverførselsreaktioner. Eksempler omfatter:
* Organiske forbindelser: Mange kulbrinter og andre organiske molekyler mangler funktionelle grupper, der ville gøre dem sure eller basiske.
* Inerte gasser: Ædelgasser er meget ureaktive og danner typisk ikke ioner.
* Salte: Mange salte dannes ved neutralisering af en syre og en base, hvilket resulterer i neutrale forbindelser. Nogle salte kan dog have sure eller basiske egenskaber afhængigt af de involverede ioner.
Opsummering: Mens mange forbindelser kan klassificeres som sure, basiske eller neutrale i specifikke sammenhænge, er det vigtigt at huske, at disse begreber er relative, og at mange forbindelser ikke passer pænt ind i disse kategorier.
Sidste artikelSyre-base-reaktioner:Forstå pH-ændringer ved blanding af syrer og baser
Næste artikelAntal atomer i Fe₂O₃:En simpel beregning
 Varme artikler
Varme artikler
-
 Ny undersøgelse af grøn te potentiale til at hjælpe med at tackle COVID-19Kredit:Unsplash/CC0 Public Domain Mens Indien fortsætter med at være hærget af pandemien, en akademiker fra Swansea University undersøger, hvordan grøn te kan give anledning til et lægemiddel, der
Ny undersøgelse af grøn te potentiale til at hjælpe med at tackle COVID-19Kredit:Unsplash/CC0 Public Domain Mens Indien fortsætter med at være hærget af pandemien, en akademiker fra Swansea University undersøger, hvordan grøn te kan give anledning til et lægemiddel, der -
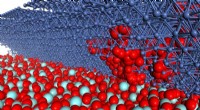 Atomisk præcise modeller forbedrer forståelsen af brændselscellerDe indledende positioner af atomerne i denne computermodel af en fast-oxid brændselscelle var baseret på observationer af den faktiske atomare konfiguration ved hjælp af elektronmikroskopi. Simulering
Atomisk præcise modeller forbedrer forståelsen af brændselscellerDe indledende positioner af atomerne i denne computermodel af en fast-oxid brændselscelle var baseret på observationer af den faktiske atomare konfiguration ved hjælp af elektronmikroskopi. Simulering -
 Beregning af kalorimetervarmen (Qcal):En praktisk vejledningAf Sean Butner, Opdateret 30. august 2022 Hesss lov understøtter bevarelsen af energi i kemiske reaktioner, idet den hævder, at den varme, der frigives eller absorberes af en reaktion, er lig med sum
Beregning af kalorimetervarmen (Qcal):En praktisk vejledningAf Sean Butner, Opdateret 30. august 2022 Hesss lov understøtter bevarelsen af energi i kemiske reaktioner, idet den hævder, at den varme, der frigives eller absorberes af en reaktion, er lig med sum -
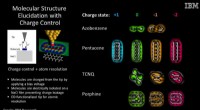 Forskere afbilder molekyler, når de ændrer ladningstilstand for første gangKredit:IBM Et team af forskere fra IBM Research-Zurich, ExxonMobil Research and Engineering Company og Universidade de Santiago de Compostela har, for første gang, afbildede molekyler, når de ændr
Forskere afbilder molekyler, når de ændrer ladningstilstand for første gangKredit:IBM Et team af forskere fra IBM Research-Zurich, ExxonMobil Research and Engineering Company og Universidade de Santiago de Compostela har, for første gang, afbildede molekyler, når de ændr


