Ionisk ledningsevne:Hvorfor faste stoffer ikke leder elektricitet - Forklaret
* Solid State: I deres faste tilstand eksisterer ioniske forbindelser som en stiv gitterstruktur. Ionerne holdes fast i faste positioner af stærke elektrostatiske kræfter. Disse kræfter begrænser ionernes bevægelse og forhindrer dem i at bære en elektrisk strøm.
* Smeltet eller vandig tilstand: Når en ionforbindelse smelter eller opløses i vand, bryder ionerne fri fra gitterstrukturen og bliver mobile. Disse mobile ioner kan nu bevæge sig frit og bære en elektrisk strøm.
Sådan virker det:
1. Elektrolyt: Når en ionforbindelse opløses i vand eller smeltes, danner den en elektrolyt . Det betyder, at den indeholder fritgående ioner, der kan lede elektricitet.
2. Elektrisk felt: Når et elektrisk felt påføres på tværs af elektrolytten, migrerer de positive ioner mod den negative elektrode (katode), og de negative ioner migrerer mod den positive elektrode (anode).
3. Elektrisk strøm: Denne bevægelse af ioner skaber en elektrisk strøm, der tillader strømmen af elektricitet gennem elektrolytten.
Opsummering: Ioniske forbindelser leder kun elektricitet, når deres ioner er frie til at bevæge sig, hvilket sker i smeltet eller opløst tilstand. I deres faste tilstand forhindrer de faste ionpositioner ledningsevne.
 Varme artikler
Varme artikler
-
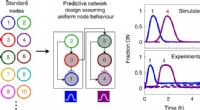 Et skridt mod skabelsen af materialer styret af kunstige generKredit:Samuel W. Schaffter et al., Nature Chemistry (2022). DOI:10.1038/s41557-022-01001-3 Vores kroppes gener arbejder sammen om at regulere, hvordan vores celler opfører sig. Hvis du f.eks. flår
Et skridt mod skabelsen af materialer styret af kunstige generKredit:Samuel W. Schaffter et al., Nature Chemistry (2022). DOI:10.1038/s41557-022-01001-3 Vores kroppes gener arbejder sammen om at regulere, hvordan vores celler opfører sig. Hvis du f.eks. flår -
 Kogende vand kan fjerne op til 90 % af mikroplastik, afslører ny undersøgelseKinga Krzeminska/Getty Images Vi modtager muligvis en kommission på køb foretaget fra links. Mikroplastik - bittesmå plastikpartikler mindre end 5 mm, som defineret af National Oceanic and Atmospher
Kogende vand kan fjerne op til 90 % af mikroplastik, afslører ny undersøgelseKinga Krzeminska/Getty Images Vi modtager muligvis en kommission på køb foretaget fra links. Mikroplastik - bittesmå plastikpartikler mindre end 5 mm, som defineret af National Oceanic and Atmospher -
 Lyser vejen til forbedrede biomaterialerKredit:Sleiman Lab Forskere fra McGill University mener, at de har fundet en måde at forbedre udviklingen af biomaterialer, der kunne være medvirkende til lægemiddellevering, vævsregenerering, n
Lyser vejen til forbedrede biomaterialerKredit:Sleiman Lab Forskere fra McGill University mener, at de har fundet en måde at forbedre udviklingen af biomaterialer, der kunne være medvirkende til lægemiddellevering, vævsregenerering, n -
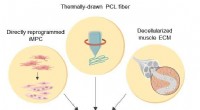 Biokonstrueret hybrid muskelfiber til regenerativ medicinSkematisk illustration af de 3D-skeletmuskellignende biomanipulerede konstruktioner Kredit:Institut for Grundvidenskab Muskler udgør det største organ hos mennesker, tegner sig for 40% af kropsmas
Biokonstrueret hybrid muskelfiber til regenerativ medicinSkematisk illustration af de 3D-skeletmuskellignende biomanipulerede konstruktioner Kredit:Institut for Grundvidenskab Muskler udgør det største organ hos mennesker, tegner sig for 40% af kropsmas
- Nedbør renser atmosfæren af støvpartikler, og efter en regnsky ser ud til at forsvinde, er diss…
- Hvordan vil du bevise, at volumen af et atom hovedsageligt er det tomme rum?
- Navngiv en bakterie, der ikke forårsager sygdom?
- Undersøgelse undersøger nanoteknologi-relateret sikkerheds- og etikproblem
- Hvorfor er kulstof vigtig for at danne disse komplicerede molekyler?
- Hvad var troen på araber om solsystemet?


