Faktorer, der påvirker kemiske reaktionshastigheder:En omfattende vejledning
1. Temperatur: Forøgelse af temperaturen øger generelt reaktionshastigheden. Dette skyldes, at højere temperaturer giver mere kinetisk energi til de reagerende molekyler, hvilket fører til hyppigere og kraftigere kollisioner, der sandsynligvis vil resultere i bindingsbrud og produktdannelse.
2. Koncentration: En højere koncentration af reaktanter fører generelt til en hurtigere reaktionshastighed. Dette skyldes, at der er flere reaktantmolekyler til stede, hvilket øger sandsynligheden for kollisioner og vellykkede reaktioner.
3. Overfladeareal: For reaktioner, der involverer faste stoffer, vil en forøgelse af overfladearealet af det faste stof generelt øge reaktionshastigheden. Dette skyldes, at mere af det faste stof udsættes for reaktanterne, hvilket giver mulighed for flere kontaktpunkter og muligheder for reaktioner. Tænk på en træblok vs. træspåner til afbrænding.
4. Katalysator: En katalysator er et stof, der fremskynder en reaktion uden at blive forbrugt i processen. Katalysatorer virker ved at give en alternativ reaktionsvej med en lavere aktiveringsenergi, hvilket betyder, at reaktionen kræver mindre energi for at starte.
 Varme artikler
Varme artikler
-
 Kemisk ingeniør udvikler styrenfrie biofornyelige harpikserPh.d.-studerende Harshal Bambhania hjælper med at udvikle nye styrenfrie biofornyelige harpikser. Kredit:Michigan State University Forskning ved Michigan State University udvikler nye styrenfrie b
Kemisk ingeniør udvikler styrenfrie biofornyelige harpikserPh.d.-studerende Harshal Bambhania hjælper med at udvikle nye styrenfrie biofornyelige harpikser. Kredit:Michigan State University Forskning ved Michigan State University udvikler nye styrenfrie b -
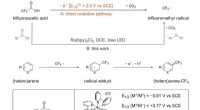 Trifluoreddikesyre virker som trifluormethyleringsmiddel i aren CH-funktionaliseringTrifluormethylering, Chlorodifluormethylering og Perfluoralkylering af Arenes. Kredit:JIN Jian Forskere ved Shanghai Institute of Organic Chemistry fra det kinesiske videnskabsakademi har udviklet
Trifluoreddikesyre virker som trifluormethyleringsmiddel i aren CH-funktionaliseringTrifluormethylering, Chlorodifluormethylering og Perfluoralkylering af Arenes. Kredit:JIN Jian Forskere ved Shanghai Institute of Organic Chemistry fra det kinesiske videnskabsakademi har udviklet -
 Metaller supplerer en lovende metode til at begrave skadeligt kuldioxid under havetKredit:CC0 Public Domain Der er en global race om at reducere mængden af skadelige gasser i vores atmosfære for at bremse tempoet i klimaændringer, og en måde at gøre det på er gennem kulstofops
Metaller supplerer en lovende metode til at begrave skadeligt kuldioxid under havetKredit:CC0 Public Domain Der er en global race om at reducere mængden af skadelige gasser i vores atmosfære for at bremse tempoet i klimaændringer, og en måde at gøre det på er gennem kulstofops -
 En lavtemperaturmetode til fremstilling af højtydende termoelektriske materialerMohamad Nugraha (til venstre) og hans gruppeleder, Derya Baran, demonstrere enhedens fleksibilitet. Kredit:KAUST Noget af den enorme mængde spildte energi, som maskiner og enheder udsender som var
En lavtemperaturmetode til fremstilling af højtydende termoelektriske materialerMohamad Nugraha (til venstre) og hans gruppeleder, Derya Baran, demonstrere enhedens fleksibilitet. Kredit:KAUST Noget af den enorme mængde spildte energi, som maskiner og enheder udsender som var
- USA ønsker en bemandet mission til månen om fem år - men kan og skal det lade sig gøre?
- Er cellerne, der bevæger vand i planter xylem eller phloem -neglebånd ingen af dem?
- Svulmende Europa seler til toppen af rekordvarmebølge
- Hvorfor ændrer levesteder?
- Hvad er et resultat af en organisme, der har meristem?
- Låner et blad fra biologien for at bevare truede sprog


