Acetone vs. Diethylether:Forståelse af kogepunktsforskelle
* Intermolekylære kræfter: Styrken af intermolekylære kræfter påvirker direkte kogepunktet. Stærkere kræfter kræver mere energi at overvinde, hvilket resulterer i et højere kogepunkt.
* Propanon (acetone): Acetone udviser primært dipol-dipol-interaktioner på grund af dens polære carbonylgruppe (C=O). Disse interaktioner er svagere end hydrogenbindinger.
* Ethoxyethan (diethylether): Diethylether har kun svage London-spredningskræfter, som er den svageste type intermolekylære kraft. Dette skyldes, at dets molekyle er upolært.
Derfor, selvom propanon har en større molekylvægt end ethoxyethan, er dens stærkere dipol-dipolkræfter stadig svagere end hydrogenbindingen, der er til stede i mange molekyler med lignende molekylvægte. Dette er grunden til, at ethoxyethan har et højere kogepunkt end propanon.
 Varme artikler
Varme artikler
-
 Legeringssammensætninger kan påvirke partiklernes elektroniske tilstandeFigur. Spektralmålinger opnået ved hjælp af højopløsningsfotoelektronspektroskopi. I disse forsøg, hård røntgensynkrotronstråling blev påført prøvepartikler. (a) og (b) viser Rh 3d kerneniveauspektre,
Legeringssammensætninger kan påvirke partiklernes elektroniske tilstandeFigur. Spektralmålinger opnået ved hjælp af højopløsningsfotoelektronspektroskopi. I disse forsøg, hård røntgensynkrotronstråling blev påført prøvepartikler. (a) og (b) viser Rh 3d kerneniveauspektre, -
 Solid-ion ledere for sikrere batterierInden for elektrokemi, det dendrit-undertrykkende domæne var endnu ikke blevet udforsket, selvom det dendrit-blokerende regime allerede var velkendt og undersøgt. Kredit:College of Engineering, Carneg
Solid-ion ledere for sikrere batterierInden for elektrokemi, det dendrit-undertrykkende domæne var endnu ikke blevet udforsket, selvom det dendrit-blokerende regime allerede var velkendt og undersøgt. Kredit:College of Engineering, Carneg -
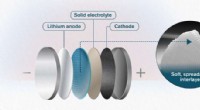 Et smørbart mellemlag kunne gøre solid state-batterier mere stabileSolid state-batterier er af stor interesse for elbilindustrien. Forskere ved Chalmers Tekniske Universitet, Sverige, og Xian Jiaotong University, Kina præsenterer nu en ny måde at bringe dette lovende
Et smørbart mellemlag kunne gøre solid state-batterier mere stabileSolid state-batterier er af stor interesse for elbilindustrien. Forskere ved Chalmers Tekniske Universitet, Sverige, og Xian Jiaotong University, Kina præsenterer nu en ny måde at bringe dette lovende -
 Forskere rapporterer om ny teknik til afisning af overfladerFotografiet viser en af de mønstrede understrukturer, som Zhang og hans kolleger brugte i designet af deres anti-isbelægning. Understrukturerne var med til at forårsage makro-revner i grænsefladen m
Forskere rapporterer om ny teknik til afisning af overfladerFotografiet viser en af de mønstrede understrukturer, som Zhang og hans kolleger brugte i designet af deres anti-isbelægning. Understrukturerne var med til at forårsage makro-revner i grænsefladen m


