Halogen-metal-kombinationer:Forståelse af saltdannelse
Her er hvorfor:
* Halogener er meget elektronegative elementer (de elsker at få elektroner).
* Metaller er elektropositive (de kan lide at miste elektroner).
Denne forskel i elektronegativitet gør dem til perfekte partnere til at danne ioniske forbindelser - en type forbindelse, hvor et atom giver en elektron til et andet for at danne modsat ladede ioner. Disse ioner tiltrækker derefter hinanden og danner et salt.
Eksempler:
* Natriumchlorid (NaCl) - Bordsalt (Natrium, et metal, giver en elektron til klor, et halogen)
* Kaliumiodid (KI) - Anvendes i kosttilskud (Kalium, et metal, giver en elektron til jod, et halogen)
* Magnesiumbromid (MgBr2) (Magnesium, et metal, giver elektroner til brom, et halogen)
Vigtig bemærkning:
Mens halogener reagerer let med de fleste metaller, er der nogle undtagelser:
* Ædelmetaller (som guld og platin) er mindre reaktive og danner ikke let salte med halogener.
* Nogle metaller kan danne mere komplekse forbindelser hvor bindingen ikke er rent ionisk, men mere kovalent af natur.
Så generelt er din udtalelse korrekt! Halogener og metaller er en vindende kombination til fremstilling af salte.
 Varme artikler
Varme artikler
-
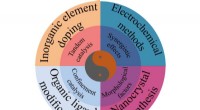 Tuningstrategier og struktureffekter af elektrokatalysatorer til kuldioxidreduktionsreaktionenForskellige afstemningsstrategier muliggør forskelle i katalysatorstrukturer. Hvordan træffer man et valg fra disse tilgængelige tuning-strategier? Der kan foretages en afvejning mellem den ønskede st
Tuningstrategier og struktureffekter af elektrokatalysatorer til kuldioxidreduktionsreaktionenForskellige afstemningsstrategier muliggør forskelle i katalysatorstrukturer. Hvordan træffer man et valg fra disse tilgængelige tuning-strategier? Der kan foretages en afvejning mellem den ønskede st -
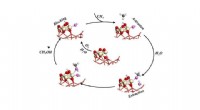 Vand er nøglen til katalytisk omdannelse af methan til methanolKatalytisk cyklus til selektiv omdannelse af methan til methanol ved at udsætte metanen for ilt og vand. Kredit:Brookhaven National Laboratory Forskere ved det amerikanske energiministerium Brookh
Vand er nøglen til katalytisk omdannelse af methan til methanolKatalytisk cyklus til selektiv omdannelse af methan til methanol ved at udsætte metanen for ilt og vand. Kredit:Brookhaven National Laboratory Forskere ved det amerikanske energiministerium Brookh -
 Forskere har opdaget, hvordan blodorme fremstiller deres unikke kobbertænderVenstre:Billede af den udbøjede snabel af Glycera dibranchiata med dens fire fritlagte kæber, højre:Scanningselektronmikroskopbillede af en Glycera-kæbe (Skalastang, 0,5 mm). Kredit:Matter/Wonderly et
Forskere har opdaget, hvordan blodorme fremstiller deres unikke kobbertænderVenstre:Billede af den udbøjede snabel af Glycera dibranchiata med dens fire fritlagte kæber, højre:Scanningselektronmikroskopbillede af en Glycera-kæbe (Skalastang, 0,5 mm). Kredit:Matter/Wonderly et -
 Hvordan ændrer denne blå blomst te farve?Kredit:The American Chemical Society Måske har du set en smuk, farveskiftende te på sociale medier. Chancerne er, det er sommerfugleærteblomstte. Denne uge, vi undersøger, hvad der gør det muligt
Hvordan ændrer denne blå blomst te farve?Kredit:The American Chemical Society Måske har du set en smuk, farveskiftende te på sociale medier. Chancerne er, det er sommerfugleærteblomstte. Denne uge, vi undersøger, hvad der gør det muligt
- Hvad sker der, når du går fra lav effekt til høj magt på et mikroskop?
- Sådan beregnes ækvivalente enheder
- Konstruktionsstabile og effektive nanopladekatalysatorer med Turing-strukturer til brintproduktion
- Hvilken farve er kobbersulfat på pH -skala?
- Hvad er de 60 videnskabsgrene?
- Hvad gjorde Galileo for at blive berømt bortset fra jordens spins omkring Sun Theory?


