Temperaturens indflydelse på opløselighed:En omfattende vejledning (100g H2O)
Generelle principper:
* Opløselighed: Opløselighed refererer til den maksimale mængde af et opløst stof (det stof, der opløses), der kan opløses i en given mængde opløsningsmiddel (normalt vand) ved en bestemt temperatur.
* Temperatur: Temperatur spiller en afgørende rolle for opløselighed. Forholdet mellem temperatur og opløselighed er forskelligt for forskellige forbindelser.
Typer af forbindelser:
* Fast:
* De fleste faste stoffer: For de fleste faste forbindelser er stigende temperatur stiger opløselighed. Dette skyldes, at højere temperaturer giver mere energi til opløsningsmiddelmolekylerne til at bryde det opløste stofs krystalgitter fra hinanden og trække dets partikler i opløsning.
* Undtagelser: Nogle faste forbindelser har omvendt opløselighed , hvilket betyder, at deres opløselighed *aftager* med stigende temperatur. Dette er mindre almindeligt, og eksempler omfatter calciumhydroxid (Ca(OH)2) og ceriumsulfat (Ce2(SO4)3).
* Gasser:
* Gasser i væsker: For gasser opløst i væsker falder stigende temperatur opløselighed. Dette skyldes, at højere temperaturer får gasmolekyler til at have mere kinetisk energi, hvilket gør dem mere tilbøjelige til at flygte fra væskefasen og vende tilbage til gasfasen.
* Eksempel: Du vil bemærke dette, når du opvarmer en sodavand eller øl; den opløste kuldioxid (CO₂) bobler ud, når temperaturen stiger.
* Væsker:
* Blandbare væsker: Væsker, der blandes fuldstændigt i alle proportioner (som alkohol og vand) har generelt en opløselighed, der er mindre påvirket af temperaturændringer.
* Imblanderbare væsker: Væsker, der ikke blandes godt (som olie og vand), vil have begrænset opløselighed, og temperaturændringer har typisk en mindre indvirkning.
100 g vand:
Mængden af vand (100 g) påvirker *mængden* af opløst stof, der kan opløses, men de generelle principper for temperaturens indflydelse forbliver de samme.
Specifikke eksempler:
* Sukker (saccharose): Forøgelse af temperaturen øger markant mængden af sukker, der kan opløses i 100 g vand.
* Salt (NaCl): Mens salt er ret opløseligt i vand, stiger dets opløselighed moderat med stigende temperatur.
* Oxygen (O₂): Når temperaturen på vand stiger, kan mindre ilt opløses i de 100 g vand.
Vigtige overvejelser:
* Tryk: For gasser spiller tryk også en væsentlig rolle for opløseligheden. Stigende tryk øger generelt opløseligheden af en gas.
* Polaritet: Polariteten af det opløste stof og opløsningsmidlet påvirker også opløseligheden. Polære opløste stoffer opløses bedre i polære opløsningsmidler (som vand), og upolære opløste stoffer opløses bedre i upolære opløsningsmidler (som olie).
Sig til, hvis du vil undersøge opløseligheden af en specifik forbindelse mere detaljeret!
Sidste artikelKI-forbindelse:Egenskaber, ionisk natur og iondannelse
Næste artikelFørende lande inden for kemisk forskning og udvikling
 Varme artikler
Varme artikler
-
 Forskere skaber en unik legering til luft, jernbanetransporterTorgom Akopyan, seniorforsker ved NUST MISIS Institut for Metalformning. Kredit:Sergey Gnuskov, SKAL IKKE MISIS Forskere fra National University of Science and Technology MISIS (NUST MISIS) i sama
Forskere skaber en unik legering til luft, jernbanetransporterTorgom Akopyan, seniorforsker ved NUST MISIS Institut for Metalformning. Kredit:Sergey Gnuskov, SKAL IKKE MISIS Forskere fra National University of Science and Technology MISIS (NUST MISIS) i sama -
 Brug af elektricitet til at nedbryde forurenende stoffer efter spildevandsrensningKredit:CC0 Public Domain Pesticider, farmaceutiske produkter, og hormonforstyrrende stoffer er nye forurenende stoffer, der ofte findes i renset husspildevand, selv efter sekundær behandling. Prof
Brug af elektricitet til at nedbryde forurenende stoffer efter spildevandsrensningKredit:CC0 Public Domain Pesticider, farmaceutiske produkter, og hormonforstyrrende stoffer er nye forurenende stoffer, der ofte findes i renset husspildevand, selv efter sekundær behandling. Prof -
 Roamingreaktioner undersøger at kaste nyt lys over atmosfæriske molekylerKredit:CC0 Public Domain En detaljeret undersøgelse af roamingreaktioner - hvor atomer af forbindelser deler sig og kredser om andre atomer for at danne uventede nye forbindelser - kunne sætte for
Roamingreaktioner undersøger at kaste nyt lys over atmosfæriske molekylerKredit:CC0 Public Domain En detaljeret undersøgelse af roamingreaktioner - hvor atomer af forbindelser deler sig og kredser om andre atomer for at danne uventede nye forbindelser - kunne sætte for -
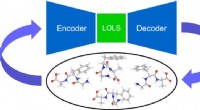 Ny maskinlæringstilgang letter molekylær konformersøgning i komplekse molekylerKredit:Aalto Universitet CEST-forskere udviklede en ny maskinlæringstilgang baseret på et lav-energi latent rum (LOLS) og densitets funktionel teori (DFT) til at søge efter molekylære konformere.
Ny maskinlæringstilgang letter molekylær konformersøgning i komplekse molekylerKredit:Aalto Universitet CEST-forskere udviklede en ny maskinlæringstilgang baseret på et lav-energi latent rum (LOLS) og densitets funktionel teori (DFT) til at søge efter molekylære konformere.
- Hvad er 3 store landformer i Frankrig?
- Hvordan ville du skelne mellem hastighed og hastighed?
- Hvordan er vand fysisk anderledes end brint og ilt?
- Wafer-skala mønstre af guld nanopartikel arrays muliggør forbedret biosensing
- Gammablazarer på himlen
- Tre til prisen for én -- mobile elektroner multipliceret i kvanteprikfilm


