Faktorer, der påvirker opløseligheden af opløste stoffer:En omfattende vejledning
1. Arten af det opløste stof og opløsningsmidlet:
* "Like opløses som": Dette princip siger, at polære opløste stoffer opløses godt i polære opløsningsmidler, og ikke-polære opløste stoffer opløses godt i upolære opløsningsmidler.
* Polære opløste stoffer: Har ujævn fordeling af elektrontæthed, hvilket skaber delvise positive og negative ladninger (f.eks. sukker, salt).
* Ikke-polære opløste stoffer: Har en jævn fordeling af elektrondensitet, ingen tydelige ladninger (f.eks. olie, fedt).
* Polære opløsningsmidler: Har molekyler med permanente dipoler (f.eks. vand, ethanol).
* Ikke-polære opløsningsmidler: Har molekyler uden permanente dipoler (f.eks. hexan, benzen).
* Intermolekylære kræfter: Styrken af tiltrækning mellem opløst stof og opløsningsmiddelmolekyler bestemmer, hvor godt de interagerer.
* Hydrogenbinding: Stærkeste intermolekylære kraft, ofte til stede i polære stoffer som vand.
* Dipol-dipolkræfter: Tiltrækning mellem polære molekyler.
* Spredningskræfter i London: Den svageste kraft, til stede i alle molekyler, stærkere i større, mere polariserbare molekyler.
2. Temperatur:
* Generelt øger stigende temperatur opløseligheden: Dette skyldes, at højere temperaturer giver mere energi til de opløste molekyler til at overvinde de intermolekylære kræfter, der holder dem sammen og brydes fra hinanden.
* Der findes undtagelser: Opløseligheden af nogle gasser falder med stigende temperatur på grund af svækkelsen af tiltrækningskræfterne mellem gasmolekylerne og opløsningsmidlet.
3. Tryk:
* Tryk påvirker primært opløseligheden af gasser:
* Henrys lov: Opløseligheden af en gas i en væske er direkte proportional med partialtrykket af gassen over væsken. Det betyder, at stigende tryk tvinger flere gasmolekyler i opløsning.
4. Partikelstørrelse:
* Mindre partikler opløses hurtigere: Mindre partikler har et større overfladeareal udsat for opløsningsmidlet, hvilket letter hurtigere interaktion og opløsning.
5. Omrøring eller omrøring:
* Omrøring eller omrøring øger opløsningshastigheden: Det bringer frisk opløsningsmiddel i kontakt med det opløste stof og erstatter den allerede mættede opløsning, der omgiver de opløste partikler, hvilket fremmer yderligere opløsning.
6. Tilstedeværelse af andre opløste stoffer:
* Tilstedeværelsen af andre opløste stoffer kan påvirke opløseligheden af et givet opløst stof:
* Fælles ioneffekt: Hvis en opløsning allerede indeholder en ion, der er fælles for det opløselige stof, kan opløseligheden af det opløste stof reduceres.
* Salteffekt: Tilstedeværelsen af salte kan påvirke opløseligheden af andre opløste stoffer, afhængigt af de specifikke interaktioner mellem de involverede ioner.
7. Specifikke løsningseffekter:
* Nogle opløste stoffer kan danne komplekser eller specifikke interaktioner med opløsningsmidlet: Disse interaktioner kan øge eller hindre opløselighed afhængigt af deres natur.
At forstå disse faktorer hjælper med at forudsige og kontrollere, hvordan et opløst stof opløses i et givet opløsningsmiddel, hvilket er afgørende for forskellige anvendelser inden for kemi, biologi og dagligdagen.
 Varme artikler
Varme artikler
-
 Paleopharmaceuticals fra baltisk rav kan bekæmpe lægemiddelresistente infektionerBaltisk rav er ikke kun smukt, men også en potentiel kilde til nye antibiotika. Kredit:Connor McDermott I århundreder, mennesker i de baltiske lande har brugt gammelt rav til medicinske formål. Se
Paleopharmaceuticals fra baltisk rav kan bekæmpe lægemiddelresistente infektionerBaltisk rav er ikke kun smukt, men også en potentiel kilde til nye antibiotika. Kredit:Connor McDermott I århundreder, mennesker i de baltiske lande har brugt gammelt rav til medicinske formål. Se -
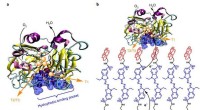 Forbedring af elektronoverførsel i enzymatiske biobrændselscellerDen som designet poly(pyrr)–ABTS–pyr film. en, Repræsentationer af Trametes versicolor Lac med den hydrofobe bindingslomme orienteret mod bunden af siden og T1 kobberstedet placeret på den ene side
Forbedring af elektronoverførsel i enzymatiske biobrændselscellerDen som designet poly(pyrr)–ABTS–pyr film. en, Repræsentationer af Trametes versicolor Lac med den hydrofobe bindingslomme orienteret mod bunden af siden og T1 kobberstedet placeret på den ene side -
 DNA-origami overskrider vigtige tærsklerI et første skridt danner forskere ved det tekniske universitet i München V-formede byggesten ved hjælp af DNA-origami-teknikker. Bestemt af åbningsvinklen samles et defineret antal byggesten selv i e
DNA-origami overskrider vigtige tærsklerI et første skridt danner forskere ved det tekniske universitet i München V-formede byggesten ved hjælp af DNA-origami-teknikker. Bestemt af åbningsvinklen samles et defineret antal byggesten selv i e -
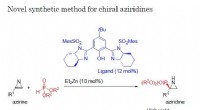 Ny kemisk syntesemetode kan producere en spændende række nye forbindelserForskere ved Nagoya Institute of Technology har etableret en reaktion katalyseret af Bis(imidazolin)/zink, hvorved 2H-aziriner reagerer med phosphit, hvilket giver aziridiner ved et højt enantiomert f
Ny kemisk syntesemetode kan producere en spændende række nye forbindelserForskere ved Nagoya Institute of Technology har etableret en reaktion katalyseret af Bis(imidazolin)/zink, hvorved 2H-aziriner reagerer med phosphit, hvilket giver aziridiner ved et højt enantiomert f
- Hvor er gammel skorpe skubbet ned i en grøft?
- Udforsker årsagerne til, at nogle kvinder bruger magt
- Hvor lang tid tager det for den nye at gå fra en måne fuldmåne?
- Hvor mange mol svovltrioxid dannes fra 3 dioxid?
- Hvad er rollen af IgM-antistoffet?
- Hvorfor kan en atlet hurtigt få mere energi ved at spise glukose snarere end stivelse?


