Syre-ammoniak-reaktioner:Forståelse af ammoniumsaltdannelse
Reaktionen:
Ammoniak (NH₃) er en svag base, mens syrer er protondonorer (H⁺). Når en syre reagerer med ammoniak, donerer syren en proton til ammoniakmolekylet og danner en ammoniumion (NH4⁺). Den negativt ladede ion fra syren kombineres derefter med ammoniumionen og danner et salt.
Eksempel:
* Saltsyre (HCl) + ammoniak (NH₃) → Ammoniumchlorid (NH₄Cl) + vand (H₂O)
Forklaring:
1. Protonoverførsel: Hydrogenionen (H+) fra HCl overføres til ammoniakmolekylet (NH3).
2. Ammoniumiondannelse: Ammoniakmolekylet accepterer protonen og bliver til en ammoniumion (NH4⁺).
3. Saltdannelse: Chloridionen (Cl⁻) fra HCl kombineres med ammoniumionen (NH4+) for at danne ammoniumchlorid (NH4Cl), et salt.
Nøglepunkter:
* Neutralisering: Reaktionen mellem en syre og en base er en neutraliseringsreaktion, der resulterer i dannelsen af salt og vand.
* Saltegenskaber: Ammoniumsalte er normalt hvide, krystallinske faste stoffer, der er opløselige i vand.
* Eksoterm reaktion: Reaktionen mellem syrer og ammoniak er normalt eksoterm og frigiver varme.
Bemærk: Syrens styrke og koncentrationen af reaktanterne kan påvirke reaktionens hastighed og omfang.
Sidste artikelForståelse af kemiske egenskaber:Hvordan produkter opstår
Næste artikelForståelse af sæbemolekyler:struktur og egenskaber
 Varme artikler
Varme artikler
-
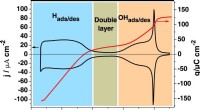 Ny forståelse af nøglebrændselscellekatalysatorTopmoderne for Pt(111). Cyklisk voltammogram (sort linje, venstre akse) og ladningstæthedskurve (rød linje, højre akse) for Pt (111) optaget i 0,1 M HClO4-opløsning ved en scanningshastighed på 50 mV
Ny forståelse af nøglebrændselscellekatalysatorTopmoderne for Pt(111). Cyklisk voltammogram (sort linje, venstre akse) og ladningstæthedskurve (rød linje, højre akse) for Pt (111) optaget i 0,1 M HClO4-opløsning ved en scanningshastighed på 50 mV -
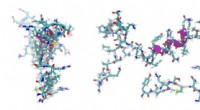 Mekanokemisk peptidbindingsdannelse bag livets oprindelseKredit:CC0 Public Domain Tilstedeværelsen af aminosyrer på den præbiotiske jord er bredt accepteret, enten kommer fra endogene kemiske processer eller leveres af udenjordisk materiale. På den an
Mekanokemisk peptidbindingsdannelse bag livets oprindelseKredit:CC0 Public Domain Tilstedeværelsen af aminosyrer på den præbiotiske jord er bredt accepteret, enten kommer fra endogene kemiske processer eller leveres af udenjordisk materiale. På den an -
 Velcro-lignende madsensor registrerer fordærv og forureningDen velcro-lignende madsensor, lavet af en række silkemikronåle, kan stikke gennem plastikemballage for at prøve mad for tegn på fordærv og bakteriel forurening. Kredit:Felice Frankel MIT ingeniør
Velcro-lignende madsensor registrerer fordærv og forureningDen velcro-lignende madsensor, lavet af en række silkemikronåle, kan stikke gennem plastikemballage for at prøve mad for tegn på fordærv og bakteriel forurening. Kredit:Felice Frankel MIT ingeniør -
 Skinnende megakrystaller, der bygger sig selvOptisk mikroskopibillede af store kubiske supergitter. Sådanne supergitter er potentielle kandidater til brug som meget energieffektive, ultrahurtige lysgivere. Kredit:Empa Et internationalt hold
Skinnende megakrystaller, der bygger sig selvOptisk mikroskopibillede af store kubiske supergitter. Sådanne supergitter er potentielle kandidater til brug som meget energieffektive, ultrahurtige lysgivere. Kredit:Empa Et internationalt hold


