Forståelse af sæbemolekyler:struktur og egenskaber
Hoved:
* Carboxylsyregruppe (-COO-)
* Denne gruppe er polær og tiltrækker vandmolekyler, hvilket gør den hydrofil.
* Ionbinding til en metalkation (f.eks. Na+, K+)
* Dette skaber et ladet hoved, hvilket yderligere øger dets opløselighed i vand.
Hale:
* Lang kulbrintekæde (typisk 12-18 kulstofatomer)
* Denne kæde er upolær og hydrofob, hvilket betyder, at den afviser vand, men tiltrækker fedt og olie.
Her er et forenklet diagram over et sæbemolekyle:
```
O
||
-C-O-Na+
|
CH3-(CH2)n-
|
...
|
CH3
```
Sådan virker det:
Den hydrofobe hale af sæbemolekylet interagerer med fedt og olie, mens det hydrofile hoved interagerer med vand. Når sæbe tilsættes vand og fedt, omgiver sæbemolekylerne fedtdråberne og danner miceller . De hydrofobe haler vender indad mod fedtet, mens de hydrofile hoveder vender udad mod vandet. Dette gør det muligt at suspendere fedtet i vand og til sidst vaskes væk.
 Varme artikler
Varme artikler
-
 Enkel arsenføler kan redde livPrototypen arsenik sensor. Kredit:Bio Nano Consulting En lavpris, brugervenlig sensor, der kan teste drikkevand for arsen på bare et minut, er blevet udviklet af Imperial- og UCL-forskere. I hele
Enkel arsenføler kan redde livPrototypen arsenik sensor. Kredit:Bio Nano Consulting En lavpris, brugervenlig sensor, der kan teste drikkevand for arsen på bare et minut, er blevet udviklet af Imperial- og UCL-forskere. I hele -
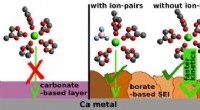 Boratbaserede passiveringslag muliggør reversible calciumbatterierFigur 1:(Venstre) Karbonatbaseret passiveringslag (dannet i Ca(TFSI) 2 baseret elektrolyt) tillader ikke plettering/stripping af calcium. (Højre) Boreret-baseret passiveringslag (dannet i Ca(BF 4
Boratbaserede passiveringslag muliggør reversible calciumbatterierFigur 1:(Venstre) Karbonatbaseret passiveringslag (dannet i Ca(TFSI) 2 baseret elektrolyt) tillader ikke plettering/stripping af calcium. (Højre) Boreret-baseret passiveringslag (dannet i Ca(BF 4 -
 Sådan navngives ioniske forbindelser – en klar, trin-for-trin guideViktorCap/iStock/GettyImages Sådan navngiver man ioniske forbindelser Når atomer deler elektroner, danner de kovalente bindinger. Når ioner med modsatte ladninger tiltrækker, skaber de ioniske forbin
Sådan navngives ioniske forbindelser – en klar, trin-for-trin guideViktorCap/iStock/GettyImages Sådan navngiver man ioniske forbindelser Når atomer deler elektroner, danner de kovalente bindinger. Når ioner med modsatte ladninger tiltrækker, skaber de ioniske forbin -
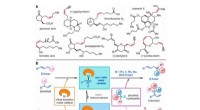 Iridium-katalyserede Z-tilbageholdende asymmetriske allyliske substitutionsreaktionerStrategi for konstruktion af Z-olefiner via asymmetriske allyliske substitutionsreaktioner katalyseret af overgangsmetalkatalysatorer. (A) Udvalgte naturlige produkter indeholdende Z-olefiner med homo
Iridium-katalyserede Z-tilbageholdende asymmetriske allyliske substitutionsreaktionerStrategi for konstruktion af Z-olefiner via asymmetriske allyliske substitutionsreaktioner katalyseret af overgangsmetalkatalysatorer. (A) Udvalgte naturlige produkter indeholdende Z-olefiner med homo
- Kan Fukushimas radioaktive vand udgøre en varig trussel mod mennesker og miljø?
- Hvad er pseudoplastmaterialer?
- Hvor er de fleste af dværgplaneterne i dit solsystem?
- En elektrisk motor konverterer elektrisk energi til potentiel energi?
- De indre farvande ser indbydende ud, når varmen rammer. Hvordan man hjælper folk med at svømme si…
- Hvad kan der ske, hvis planter og organismer narres til at tænke foråret?


