Forståelse af hydrogen- og hydroxidion-forhold ved pH 4
* pH 4 er sur: En pH på 4 indikerer en sur opløsning.
* Brintioner dominerer: I sure opløsninger er koncentrationen af hydrogenioner (H+) højere end koncentrationen af hydroxidioner (OH-).
* Forholdet er logaritmisk: pH-skalaen er logaritmisk, hvilket betyder, at hver heltalsændring i pH repræsenterer en tidobbel ændring i koncentrationen af H+-ioner.
* Beregning: Da pH er 4, er koncentrationen af H+ ioner 10^-4 mol pr. liter. Vi kan finde koncentrationen af OH-ioner ved at bruge følgende forhold (ved 25°C):
* Kw (ionproduktkonstant for vand) =[H+][OH-] =10^-14
* [OH-] =Kw / [H+] =10^-14 / 10^-4 =10^-10 mol pr. liter
Opsummering:
* En opløsning med pH 4 har en meget højere koncentration af hydrogenioner (10^-4 M) sammenlignet med hydroxidioner (10^-10 M).
* Forholdet mellem H+ og OH-ioner er 10.000 til 1.
 Varme artikler
Varme artikler
-
 Hvordan varme og sollys påvirker poolens klorniveauerSirirak/iStock/GettyImages Der er intet som en forfriskende dukkert i en pool på en varm, solrig dag. Takket være klor kan du nyde krystalklart vand uden at bekymre dig om alger eller bakterier. Klor
Hvordan varme og sollys påvirker poolens klorniveauerSirirak/iStock/GettyImages Der er intet som en forfriskende dukkert i en pool på en varm, solrig dag. Takket være klor kan du nyde krystalklart vand uden at bekymre dig om alger eller bakterier. Klor -
 Nyt additiv giver brandbeskyttelse til træLaserskårne dekorative træ- og HPL-elementer kan nu udstyres med brandsikring. Kredit:Bruag AG Kravene til brandbeskyttelse er stigende på verdensplan – især i offentlige bygninger og køretøjskons
Nyt additiv giver brandbeskyttelse til træLaserskårne dekorative træ- og HPL-elementer kan nu udstyres med brandsikring. Kredit:Bruag AG Kravene til brandbeskyttelse er stigende på verdensplan – især i offentlige bygninger og køretøjskons -
 Forskere løser det 100-årige metallurgipuslespilFor at forstå præcis, hvordan metaller reagerer på højhastighedskomprimering i molekylære dynamiksimuleringer, LLNL -forskere bruger nye metoder til silikomikroskopi til at afsløre defekter i krystalg
Forskere løser det 100-årige metallurgipuslespilFor at forstå præcis, hvordan metaller reagerer på højhastighedskomprimering i molekylære dynamiksimuleringer, LLNL -forskere bruger nye metoder til silikomikroskopi til at afsløre defekter i krystalg -
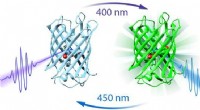 Ny teknik, der viser, hvordan en proteinlyskontakt virker, kan forbedre den biologiske forskningDette billede viser, hvordan Dronpa-lyskontakten kan tændes eller slukkes ved at bruge forskellige lysfarver (ved 400 eller 450 nm). Kredit:Stony Brook University Sollys er afgørende for alt liv,
Ny teknik, der viser, hvordan en proteinlyskontakt virker, kan forbedre den biologiske forskningDette billede viser, hvordan Dronpa-lyskontakten kan tændes eller slukkes ved at bruge forskellige lysfarver (ved 400 eller 450 nm). Kredit:Stony Brook University Sollys er afgørende for alt liv,
- Videnskabsprojekt: Hvilke mærker af korn er langest?
- Hvilke typer kernekræfter bestemmer den hastighed, hvormed et radioaktivt materiale henfalder?
- Ikke-line-of-sight rekonstruktion med signal-objekt kollaborativ regularisering
- Er temperaturen den samlede gravitationspotentiale energi i et element?
- Hvordan sociale medier hjælper videnskabsfolk med at få budskabet igennem
- Hvad er ti kemiske stoffer i supermarkedet?


