Smeltepunktstendenser i gruppe 7-elementer:Atomantal &intermolekylære kræfter
* Generel tendens: Smeltepunkter stiger generelt når du bevæger dig ned i gruppe 7 fra fluor (F) til astatin (At).
* Forklaring: Denne tendens skyldes primært stigende intermolekylære kræfter. Når du bevæger dig ned i gruppen, bliver atomerne større, med flere elektroner og en større polariserbarhed. Dette fører til stærkere London Dispersion Forces (LDF'er) mellem molekylerne, hvilket kræver mere energi for at bryde dem fra hinanden og smelte stoffet.
* Undtagelser:
* Fluor (F) har et usædvanligt lavt smeltepunkt sammenlignet med de andre halogener. Dette tilskrives dens lille størrelse og den stærke elektronegativitet af fluor, hvilket fører til svage LDF'er.
* Klor (Cl) og Brom (Br) har relativt ens smeltepunkter. Dette skyldes sandsynligvis balancen mellem de stigende LDF'er og den faldende elektronegativitet, som kan svække dipol-dipol-interaktioner.
Opsummering:
Selvom der er en generel tendens til stigende smeltepunkter ned ad gruppe 7, er forholdet ikke enkelt, og der er bemærkelsesværdige undtagelser. Smeltepunktet er påvirket af forskellige faktorer, herunder:
* Intermolekylære kræfter: Styrken af London Dispersion Forces (LDF'er) spiller en stor rolle.
* Atomstørrelse: Større atomer har generelt stærkere LDF'er.
* Elektronegativitet: Høj elektronegativitet kan påvirke styrken af dipol-dipol-interaktioner.
 Varme artikler
Varme artikler
-
 Forståelse af rustdannelse:kemi, årsager og forebyggelseAf Julie Richards — Opdateret 30. august 2022 Rust er en naturligt forekommende forbindelse, der dannes, når jern eller stål reagerer med ilt og vand. Den underliggende kemiske ligning er 4Fe + 3O₂ =
Forståelse af rustdannelse:kemi, årsager og forebyggelseAf Julie Richards — Opdateret 30. august 2022 Rust er en naturligt forekommende forbindelse, der dannes, når jern eller stål reagerer med ilt og vand. Den underliggende kemiske ligning er 4Fe + 3O₂ = -
 Oprettelse af mRNA med en helt kemisk proces kan give mulighed for tilpassede mRNA-vaccinermRNA med sin glødende hætte. Kredit:Reiko Matsushita Forskere ved Nagoya University i Japan har udviklet en ny kemisk proces, der kan repræsentere et vigtigt gennembrud i at skabe skræddersyede mRN
Oprettelse af mRNA med en helt kemisk proces kan give mulighed for tilpassede mRNA-vaccinermRNA med sin glødende hætte. Kredit:Reiko Matsushita Forskere ved Nagoya University i Japan har udviklet en ny kemisk proces, der kan repræsentere et vigtigt gennembrud i at skabe skræddersyede mRN -
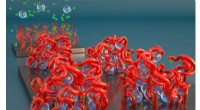 Opdager og krymper børsterne af polyelektrolytbørsterPolyelektrolytbørster illustration:I forgrunden, kraftige ioner i løsning, vist som kugler, få børstens børster til at falde sammen som klistret spaghetti. I baggrunden, blidere ioner i opløsning får
Opdager og krymper børsterne af polyelektrolytbørsterPolyelektrolytbørster illustration:I forgrunden, kraftige ioner i løsning, vist som kugler, få børstens børster til at falde sammen som klistret spaghetti. I baggrunden, blidere ioner i opløsning får -
 Forskere udvikler verdens første alkoholiske drik lavet af tofuvalleLektor Liu Shao Quan (til højre) og ph.d.-studerende Mr. Chua Jian Yong (til venstre), begge fra Fødevarevidenskab &Teknologiuddannelsen under NUS Det Naturvidenskabelige Fakultet, med succes forvandl
Forskere udvikler verdens første alkoholiske drik lavet af tofuvalleLektor Liu Shao Quan (til højre) og ph.d.-studerende Mr. Chua Jian Yong (til venstre), begge fra Fødevarevidenskab &Teknologiuddannelsen under NUS Det Naturvidenskabelige Fakultet, med succes forvandl
- Hvilket botanik -fænomen er primært baseret på en forståelse af fysik?
- Beskyttelse af søfarende og den globale forsyningskæde under COVID-19
- Krop, hvordan det fungerer at donere dit til videnskab
- Hvad er et mål for hvor meget elektrisk energi hvert elektronbatteri har?
- Når jorden er i den position, der er vist, der tegner nedenfor, hvilken sæson den nordlige halvkug…
- Kosmisk teoretiker og planetjægere deler fysikprisen, når nobels belønner overjordiske opdagelser


