Ioniske vs. kovalente bindinger:Analyse af Ca-Cl-bindingen
* Elektronegativitetsforskel: Calcium har en lav elektronegativitet (ca. 1,0), mens klor har en høj elektronegativitet (ca. 3,0). Forskellen i elektronegativitet er ret stor (2,0), hvilket indikerer en stærk tendens for klor til at tiltrække de delte elektroner.
* Overførsel af elektroner: På grund af denne elektronegativitetsforskel mister Calcium let to elektroner for at opnå en stabil ædelgaskonfiguration. Klor får en elektron for at opnå det samme. Denne overførsel af elektroner skaber en positiv calciumion (Ca²⁺) og en negativ chloridion (Cl⁻).
* Elektrostatisk tiltrækning: De modsatte ladninger af ionerne tiltrækker så hinanden gennem elektrostatiske kræfter og danner en ionbinding.
Sammenfattende gør den store elektronegativitetsforskel og overførslen af elektroner, der fører til dannelsen af modsat ladede ioner, bindingen mellem Calcium og Chlorionisk.
Sidste artikelEr MgCl2 ionisk eller kovalent? Forståelse af kemisk binding
Næste artikelTransparente stoffer:En omfattende liste efter stat
 Varme artikler
Varme artikler
-
 Bioluminescerende succinat -detektion overvåger dioxygenaser og JMJC -demethylaserDemethylering af DNA og Histon i Nucleosome af Demethylases. Kredit:Promega Corporation En ny (og frit tilgængelig) original forskningsartikel offentliggjort forud for print kl SLAS Discovery On
Bioluminescerende succinat -detektion overvåger dioxygenaser og JMJC -demethylaserDemethylering af DNA og Histon i Nucleosome af Demethylases. Kredit:Promega Corporation En ny (og frit tilgængelig) original forskningsartikel offentliggjort forud for print kl SLAS Discovery On -
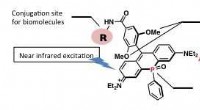 Et nær-infrarødt fluorescerende farvestof til langsigtet biobilleddannelseMolekylær struktur af det nye nær-infrarøde fluorescerende mærkningsmiddel PREX 710 med et koblingssted for et biomolekyle. Inkorporering af den elektrontiltrækkende phosphinoxid (P=O)-del i xanthenst
Et nær-infrarødt fluorescerende farvestof til langsigtet biobilleddannelseMolekylær struktur af det nye nær-infrarøde fluorescerende mærkningsmiddel PREX 710 med et koblingssted for et biomolekyle. Inkorporering af den elektrontiltrækkende phosphinoxid (P=O)-del i xanthenst -
 Automatiseret optimering og syntese af lægemidler i skyenKredit:Angewandte Chemie International Edition Shopping på internettet, lagring af billeder i skyen, skruer op for en termostat med en app – alt er almindeligt. Nu, tingenes internet og skyen komm
Automatiseret optimering og syntese af lægemidler i skyenKredit:Angewandte Chemie International Edition Shopping på internettet, lagring af billeder i skyen, skruer op for en termostat med en app – alt er almindeligt. Nu, tingenes internet og skyen komm -
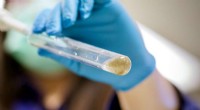 Salttolerante bakterier med appetit på slam laver biologisk nedbrydeligt plastZobellella denitrificans ZD1-bakterier lever af slam (begge vist i reagensglas) for at fremstille bionedbrydelig bioplast. Kredit:Dr. Kung-Hui (Bella) Chu USA genererer syv millioner tons spildeva
Salttolerante bakterier med appetit på slam laver biologisk nedbrydeligt plastZobellella denitrificans ZD1-bakterier lever af slam (begge vist i reagensglas) for at fremstille bionedbrydelig bioplast. Kredit:Dr. Kung-Hui (Bella) Chu USA genererer syv millioner tons spildeva
- Mestring af Codon Chart:En klar guide til at oversætte DNA til proteiner
- Hvad er et stof, der fremskynder kemisk proces?
- Kan du se Mælkevejen med nøgen øje?
- ESA stiller uret efter fjerne, roterende stjerner
- Hvad er Jordens nøjagtige tyngdekraft?
- Faster alle økosystemer de generelle træk til at overleve?


