Elektrolytopløsning:Forståelse af iondannelse i vand
Her er hvorfor:
* Elektrolytter er stoffer, der leder elektricitet, når de opløses i vand. Dette skyldes, at de dissocierer til ladede partikler kaldet ioner.
* ioner er atomer eller molekyler, der har fået eller mistet elektroner, hvilket giver dem en netto positiv eller negativ ladning.
* Når en elektrolyt opløses i vand, omgiver vandmolekylerne ionerne og trækker dem fra hinanden og bryder ionbindingerne.
* Den resulterende opløsning indeholder fritgående ioner, hvilket gør det muligt for opløsningen at lede elektricitet.
Eksempel:
Natriumchlorid (NaCl) er en elektrolyt. Når det opløses i vand, opløses det i natriumioner (Na+) og chloridioner (Cl-):
NaCl(s) → Na+(aq) + Cl-(aq)
"Aq" angiver, at ionerne er opløst i vand (vandig opløsning).
Sidste artikelMgO Dannelsesvarme:Definition &Værdi
Næste artikelMetalreaktioner med ilt:Forståelse af reaktivitetsmønstre
 Varme artikler
Varme artikler
-
 Åbning af nye døre:Første syntetiske mekanofølsomme kaliumkanalKredit:Kohei Sato, Tokyo Institute of Technology Forbløffet af egenskaberne af ionkanalproteiner, der almindeligvis observeres i celler, har Tokyo Tech-forskere udviklet den første syntetiske mekan
Åbning af nye døre:Første syntetiske mekanofølsomme kaliumkanalKredit:Kohei Sato, Tokyo Institute of Technology Forbløffet af egenskaberne af ionkanalproteiner, der almindeligvis observeres i celler, har Tokyo Tech-forskere udviklet den første syntetiske mekan -
 Innovativt biobaseret luftfilter kunne transformere luftfiltrering, eventuelt reducere luftbårne al…En mand skifter et luftfilter i en ovn. Andrew Huang, en kandidatstuderende ved Purdue University School of Industrial Engineering, har udviklet et nyt sojafilteralternativ, der fjerner specifikke par
Innovativt biobaseret luftfilter kunne transformere luftfiltrering, eventuelt reducere luftbårne al…En mand skifter et luftfilter i en ovn. Andrew Huang, en kandidatstuderende ved Purdue University School of Industrial Engineering, har udviklet et nyt sojafilteralternativ, der fjerner specifikke par -
 Forskere opdager en ny måde at målrette mod lægemiddelresistente bakterier påMethicillin-resistent Staphylococcus aureus . Kredit:NIH/NIAID John Innes Center-forskere er blandt et internationalt hold, der har opdaget en ny klasse af forbindelser, der målretter mod bakter
Forskere opdager en ny måde at målrette mod lægemiddelresistente bakterier påMethicillin-resistent Staphylococcus aureus . Kredit:NIH/NIAID John Innes Center-forskere er blandt et internationalt hold, der har opdaget en ny klasse af forbindelser, der målretter mod bakter -
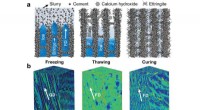 Træ-inspireret cement med høj styrke og multifunktionalitetDannelse og 3D-arkitektur af trælignende cement. a) Skematiske illustrationer af dannelsesmikromekanismerne af den trælignende cement under frysningen, optøning, og hærdningsprocesser. b) XRT-volumeng
Træ-inspireret cement med høj styrke og multifunktionalitetDannelse og 3D-arkitektur af trælignende cement. a) Skematiske illustrationer af dannelsesmikromekanismerne af den trælignende cement under frysningen, optøning, og hærdningsprocesser. b) XRT-volumeng
- Hvorfor er kroppen afhængig af glukose end lipider for energi?
- Tyve døde som rekordstor regn i Japan foranlediger masseevakuering
- Hvad betyder et højt antal på pH -skalaen?
- Undersøgelsen har til formål at give en nøjagtig vurdering af virkningen af fremtidige havnivea…
- NASA rapporterer problemer med Hubble Space Telescope
- Hvordan kaosteori virker


