Kovalente bindinger i SO₂:Forståelse af kemisk binding
* Elektronegativitet: Svovl og oxygen har relativt høje elektronegativitetsværdier, hvilket betyder, at de begge har en stærk tiltrækning af elektroner.
* Deling af elektroner: I stedet for at det ene atom fuldstændigt tager en elektron fra det andet (ionisk binding), deler svovl og ilt elektroner for at opnå en stabil elektronkonfiguration.
* Polær kovalent: Elektronegativitetsforskellen mellem svovl og oxygen er signifikant nok til, at bindingerne betragtes som polær kovalent . Det betyder, at elektronerne ikke deles ligeligt, hvor oxygenatomerne har en svagt negativ ladning og svovlatomet en let positiv ladning.
Opsummering: De kemiske bindinger i SO₂ dannes gennem deling af elektroner mellem svovl- og oxygenatomer, hvilket gør dem til kovalente bindinger .
 Varme artikler
Varme artikler
-
 Kubeformede jern-svovl-klynger understøtter multiple bindinger mellem jern og nitrogenKredit:Wiley I en række biologiske processer, jern-svovlklynger spiller en afgørende rolle, hvor de fungerer som cofaktorer til enzymer. Forskning offentliggjort i Angewandte Chemie viser nu, at
Kubeformede jern-svovl-klynger understøtter multiple bindinger mellem jern og nitrogenKredit:Wiley I en række biologiske processer, jern-svovlklynger spiller en afgørende rolle, hvor de fungerer som cofaktorer til enzymer. Forskning offentliggjort i Angewandte Chemie viser nu, at -
 Konvertering af atomer til gram:en trin-for-trin guideEmilija Randjelovic/iStock/GettyImages I kemi er oversættelse af et antal atomer til masse en grundlæggende færdighed, der understøtter mere avancerede kvantitative analyser. Konverteringen afhænger
Konvertering af atomer til gram:en trin-for-trin guideEmilija Randjelovic/iStock/GettyImages I kemi er oversættelse af et antal atomer til masse en grundlæggende færdighed, der understøtter mere avancerede kvantitative analyser. Konverteringen afhænger -
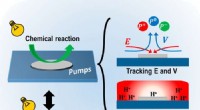 Mikropumper som en platform til forståelse af kemisk drevne mikromotorerKredit:Catalan Institute of Nanoscience and Nanotechnology Udviklingen af selvkørende mikro- og nanomaskiner, der er i stand til at efterligne den menneskelige krops og/eller det naturlige miljø
Mikropumper som en platform til forståelse af kemisk drevne mikromotorerKredit:Catalan Institute of Nanoscience and Nanotechnology Udviklingen af selvkørende mikro- og nanomaskiner, der er i stand til at efterligne den menneskelige krops og/eller det naturlige miljø -
 Mælkeprotein kan hjælpe med at øge blåbærs sundhedEn modnende Polaris blåbær (Vaccinium corymbosum) Kredit:Public Domain At parre blåbærtærte med en kugle is er en dejlig sommeroplevelse. Udover at være velsmagende, denne kombination kan også hjæ
Mælkeprotein kan hjælpe med at øge blåbærs sundhedEn modnende Polaris blåbær (Vaccinium corymbosum) Kredit:Public Domain At parre blåbærtærte med en kugle is er en dejlig sommeroplevelse. Udover at være velsmagende, denne kombination kan også hjæ
- Forskere udtænker en billigere og hurtigere måde at kontinuerligt producere aminer på
- Statistisk analyse har til formål at løse det græske vulkanmysterium
- Uddybende spørgsmål:Hvorfor overlevede pattedyr 'K/T-udryddelsen'?
- Ny mekanisme for elektronspredning i grafenlignende 2-D-materialer
- Hvilken type energi opbevares i kernen et atom?
- Forsker udforsker, hvordan universet skaber fornuft, moral


