Molekylære vs. empiriske formler:Forståelse af forskellen og forholdet
Empirisk formel
* Definition: Den empiriske formel repræsenterer det enkleste hele talforhold mellem atomer i en forbindelse.
* Eksempel: Glucose har en molekylformel på C₆H₁₂O6. Dens empiriske formel er CH2O, da forholdet mellem carbon-, hydrogen- og oxygenatomer er 1:2:1.
Molekylær formel
* Definition: Molekylformlen viser det faktiske antal atomer af hvert grundstof i et molekyle.
* Eksempel: Glucoses molekylformel (C₆H₁₂O6) fortæller os, at den indeholder 6 carbonatomer, 12 hydrogenatomer og 6 oxygenatomer.
Forhold
* Den empiriske formel er en forenklet version af den molekylære formel. Det giver det grundlæggende forhold mellem atomer, men fortæller dig ikke nødvendigvis det faktiske antal atomer i et molekyle.
* Den molekylære formel er et multiplum af den empiriske formel. For at finde molekylformlen ud fra den empiriske formel skal du kende forbindelsens molære masse. Du beregner den empiriske formelmasse og dividerer den molære masse med den empiriske formelmasse. Resultatet fortæller dig, hvor mange gange den empiriske formel gentages i molekylformlen.
Eksempel:
1. Empirisk formel: CH2O
2. Molar masse: 180 g/mol
3. Empirisk formelmasse: 12 g/mol (C) + 2 g/mol (H) + 16 g/mol (O) =30 g/mol
4. Flere: 180 g/mol / 30 g/mol =6
5. Molekylformel: (CH20)6 =C6H1206
Opsummering:
* Den empiriske formel giver det enkleste forhold mellem atomer i en forbindelse.
* Molekylformlen giver det faktiske antal atomer i et molekyle.
* Den molekylære formel er et multiplum af den empiriske formel.
 Varme artikler
Varme artikler
-
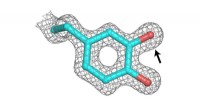 Patogener kan unddrage sig immunrespons med metalfrit enzym, der kræves til DNA-replikationEn metalfri ribonukleotidreduktase - et enzym, der kræves til DNA-replikation - fra bakterielle patogener bruger en post-translationelt modificeret aminosyre (billedet) til at starte en essentiel DNA-
Patogener kan unddrage sig immunrespons med metalfrit enzym, der kræves til DNA-replikationEn metalfri ribonukleotidreduktase - et enzym, der kræves til DNA-replikation - fra bakterielle patogener bruger en post-translationelt modificeret aminosyre (billedet) til at starte en essentiel DNA- -
 Mod 4D-print med strukturelle farverFarven på den blå tarantel (Poecilotheria metallica) kommer fra præcist arrangerede nanokrystaller. Det krystallinske array fungerer som et spejl, der kun reflekterer en bestemt bølgelængde af indkomm
Mod 4D-print med strukturelle farverFarven på den blå tarantel (Poecilotheria metallica) kommer fra præcist arrangerede nanokrystaller. Det krystallinske array fungerer som et spejl, der kun reflekterer en bestemt bølgelængde af indkomm -
 Forskere kortlægger giftige proteiner forbundet med AlzheimersRashik Ahmed, hovedforfatter og ph.d.-kandidat i Institut for Biokemi og Biomedicinske Videnskaber og Giuseppe Melacini, seniorforfatter og professor i afdelingerne for kemi og kemisk biologi Kredit:G
Forskere kortlægger giftige proteiner forbundet med AlzheimersRashik Ahmed, hovedforfatter og ph.d.-kandidat i Institut for Biokemi og Biomedicinske Videnskaber og Giuseppe Melacini, seniorforfatter og professor i afdelingerne for kemi og kemisk biologi Kredit:G -
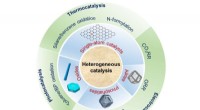 Ny anmeldelse fremhæver innovative katalysatorer:Design og anvendelseNanokatalyse spiller en afgørende rolle i den kemiske industri. Men nanokatalyse står nu over for en stor udfordring og kræver en stor revolution for at opfylde behovene i et bæredygtigt samfund. Med
Ny anmeldelse fremhæver innovative katalysatorer:Design og anvendelseNanokatalyse spiller en afgørende rolle i den kemiske industri. Men nanokatalyse står nu over for en stor udfordring og kræver en stor revolution for at opfylde behovene i et bæredygtigt samfund. Med
- Hvad er iste en sammensat blanding eller grundstof?
- Hvordan sammenligner størrelsen på, hvordan kraft udøves af jordens tyngdekraft på en bil, med u…
- Sådan beregnes volumen ved hjælp af densitet
- Hvorfor er jorden ikke i termisk ligevægt med solen?
- Hvordan konverteres hydro -strøm til elektricitet?
- Hvad er 10 forskellige faste husholdningsstoffer?


