Isotoper:ligheder og forskelle forklaret
Ligheder og forskelle mellem isotoper
Isotoper er atomer af det samme grundstof, der har det samme antal protoner (atomnummer) men forskelligt antal neutroner . Det betyder:
Ligheder:
* Samme kemiske egenskaber: Isotoper af samme grundstof har det samme antal protoner og elektroner, som bestemmer deres kemiske adfærd. De vil reagere på samme måde med andre elementer.
* Samme atomnummer: Dette er den definerende karakteristik af et element.
* Samme position i det periodiske system: Alle isotoper af et grundstof indtager samme sted i det periodiske system.
Forskelle:
* Andet massetal: Massetallet er summen af protoner og neutroner. Da isotoper har forskellige antal neutroner, har de forskellige massetal.
* Forskellig atommasse: Atommasse er det vægtede gennemsnit af masserne af alle isotoper af et grundstof. Det er derfor, at atommasser i det periodiske system ikke er hele tal.
* Forskellige fysiske egenskaber: Mens kemiske egenskaber er de samme, kan nogle fysiske egenskaber være lidt forskellige, såsom massefylde, smeltepunkt og kogepunkt.
* Forskellig nuklear stabilitet: Nogle isotoper er radioaktive, hvilket betyder, at de er ustabile og henfalder over tid. Andre isotoper er stabile.
Her er et eksempel:
* Carbon-12: 6 protoner, 6 neutroner (stabil)
* Carbon-14: 6 protoner, 8 neutroner (radioaktiv)
Både kulstof-12 og kulstof-14 er isotoper af kulstof. De har de samme kemiske egenskaber, men kulstof-14 er radioaktivt og har et andet massetal og atommasse.
Opsummering:
Isotoper er grundlæggende det samme element, men adskiller sig i deres antal neutroner, hvilket fører til variationer i masseantal, atommasse og nogle gange nuklear stabilitet og fysiske egenskaber.
 Varme artikler
Varme artikler
-
 Forskere overvinder barrierer for funktionalisering af bioinspirerede høstmaterialer fra solenergiKredit:Topbillede tilpasset fra Journal of Physical Chemical Letters. Nederste billede, Kara Ng, Naturkemi 2020 Inspireret af naturen, forskere ved City College i New York (CCNY) kan demonstrere
Forskere overvinder barrierer for funktionalisering af bioinspirerede høstmaterialer fra solenergiKredit:Topbillede tilpasset fra Journal of Physical Chemical Letters. Nederste billede, Kara Ng, Naturkemi 2020 Inspireret af naturen, forskere ved City College i New York (CCNY) kan demonstrere -
 Funktionaliserede overflader:Cylindriske micellære børster med skræddersyede kemiske muligheder m…Frøet vækst af hydrofobiske PFS53-b-PDMS418 micellære børster på en siliciumwafer. (A) Skematisk illustration af processen, som involverer immobilisering af PFS36-b-P2VP502 frø (Ln =139 nm, Lw/Ln =1,0
Funktionaliserede overflader:Cylindriske micellære børster med skræddersyede kemiske muligheder m…Frøet vækst af hydrofobiske PFS53-b-PDMS418 micellære børster på en siliciumwafer. (A) Skematisk illustration af processen, som involverer immobilisering af PFS36-b-P2VP502 frø (Ln =139 nm, Lw/Ln =1,0 -
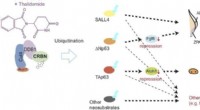 Molekylær basis for lægemiddelvirkninger på lemmer og øreudvikling afsløretThalidomid binder sig til cereblon (CRBN) og forårsager unormal lem- og øreudvikling ved at fremkalde nedbrydning af proteiner kaldet? Np63α og TAp63α gennem en proces kendt som ubiquitination. Denne
Molekylær basis for lægemiddelvirkninger på lemmer og øreudvikling afsløretThalidomid binder sig til cereblon (CRBN) og forårsager unormal lem- og øreudvikling ved at fremkalde nedbrydning af proteiner kaldet? Np63α og TAp63α gennem en proces kendt som ubiquitination. Denne -
 Producerer praktiske geler fra et protein, der findes i menneskeblodUndersøgelsen ledet af Dariush Hinderberger er forsidehistorien til det seneste nummer af Biomaterialevidenskab . Kredit:Biomaterials Science / Royal Society of Chemistry Proteinet albumin er an
Producerer praktiske geler fra et protein, der findes i menneskeblodUndersøgelsen ledet af Dariush Hinderberger er forsidehistorien til det seneste nummer af Biomaterialevidenskab . Kredit:Biomaterials Science / Royal Society of Chemistry Proteinet albumin er an
- Log-periodiske kvanteoscillationer og diskret skala-invariance i Dirac-materialer
- Forståelse af spontane redoxreaktioner:Betingelser og krav
- Serendipity udvider mulighederne for fremstilling af grafit
- Hvornår begyndte jorderosion i Australien?
- Planter & Dyr i Løvfældende Skove
- Hvilken sygdom forårsager baciller bakterier?


