Forståelse af spontane redoxreaktioner:Betingelser og krav
1. Forskel i elektronegativitet:
* De to elementer skal have en signifikant forskel i elektronegativitet.
* Grundstoffet med højere elektronegativitet vil have tendens til at få elektroner (reduktion), og grundstoffet med lavere elektronegativitet vil have tendens til at miste elektroner (oxidation).
2. Gunstig Gibbs Free Energy Change:
* Den samlede Gibbs frie energiændring (ΔG) for reaktionen skal være negativ. Dette indikerer, at reaktionen er spontan og vil forløbe uden ekstern energitilførsel.
* Gibbs frie energiændring er relateret til standardelektrodepotentialerne (E°) for de to elementer:
* ΔG =-nFE°
* hvor n er antallet af elektroner, der overføres i reaktionen, F er Faradays konstant, og E° er standardcellepotentialet.
3. Passende betingelser:
* Reaktionen kan kræve specifikke forhold som temperatur, pH eller tilstedeværelse af en katalysator for at forløbe med en rimelig hastighed.
Eksempel:
Overvej reaktionen mellem kobber (Cu) og sølv (Ag) .
* Cu har en lavere elektronegativitet end Ag .
* Standardelektrodepotentialet (E°) for Cu²⁺/Cu er +0,34 V, mens det for Ag⁺/Ag er +0,80 V.
* Derfor Ag vil blive reduceret (forstærke elektroner) og Cu vil blive oxideret (miste elektroner).
* Den overordnede reaktion er:
* Cu(s) + 2Ag⁺(aq) → Cu²⁺(aq) + 2Ag(s)
* Standardcellepotentialet (E°) for denne reaktion er +0,46 V, hvilket gør ΔG negativ.
Konklusion:
En spontan redoxreaktion mellem to grundstoffer vil dannes, hvis grundstoffet med højere elektronegativitet let kan acceptere elektroner fra grundstoffet med lavere elektronegativitet, hvilket fører til en negativ Gibbs fri energiændring.
 Varme artikler
Varme artikler
-
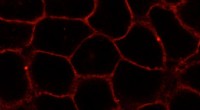 Hvordan forskere analyserer cellemembranerEn ny forbindelse, der efterligner naturligt kolesterol i membraner af levende celler (her:HeLa-celler). Stoffet er mærket med et fluorescerende farvestof (rødt). Kredit:L. Rakers et al./ Cell Chem B
Hvordan forskere analyserer cellemembranerEn ny forbindelse, der efterligner naturligt kolesterol i membraner af levende celler (her:HeLa-celler). Stoffet er mærket med et fluorescerende farvestof (rødt). Kredit:L. Rakers et al./ Cell Chem B -
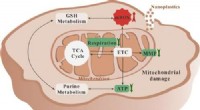 Nanoplast kan forstyrre menneskelige lever- og lungecelleprocesser i laboratorieeksperimenterGrafisk abstrakt. Kredit:Environmental Science &Technology (2022). DOI:10.1021/acs.est.2c03980 Hvad sker der, når folk ubevidst spiser, drikker eller inhalerer næsten usynlige plastikstykker? Selvo
Nanoplast kan forstyrre menneskelige lever- og lungecelleprocesser i laboratorieeksperimenterGrafisk abstrakt. Kredit:Environmental Science &Technology (2022). DOI:10.1021/acs.est.2c03980 Hvad sker der, når folk ubevidst spiser, drikker eller inhalerer næsten usynlige plastikstykker? Selvo -
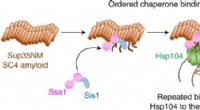 Tre ledsagere koordinerer opdelingen af amyloidfibriller i gærKredit:Yoshiko Nakagawa et al., Nature Chemical Biology (2022). DOI:10.1038/s41589-021-00951-y I et fund, der har vigtige konsekvenser for neurodegenerative lidelser såsom Alzheimers sygdom, har RI
Tre ledsagere koordinerer opdelingen af amyloidfibriller i gærKredit:Yoshiko Nakagawa et al., Nature Chemical Biology (2022). DOI:10.1038/s41589-021-00951-y I et fund, der har vigtige konsekvenser for neurodegenerative lidelser såsom Alzheimers sygdom, har RI -
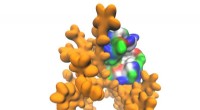 Forskere skaber multifunktionelle protein-polymerfilmDendrimer-molekyle er markeret gult. Overfladen af proteinmolekylet er farvekodet i overensstemmelse med de kemiske egenskaber af aminosyrerester (rød - positiv ladning, blå -- negativ ladning, grøn
Forskere skaber multifunktionelle protein-polymerfilmDendrimer-molekyle er markeret gult. Overfladen af proteinmolekylet er farvekodet i overensstemmelse med de kemiske egenskaber af aminosyrerester (rød - positiv ladning, blå -- negativ ladning, grøn
- En enhed til tidlig opdagelse af visse synsproblemer
- En neandertalertand opdaget i Serbien afslører menneskets migrationshistorie
- Prokaryote celler:Forstå celler uden en kerne
- Hvordan finder du nettokraften for to objekter, der virker i samme retning?
- Hvad hedder det, når bremsen ned og slides væk fra Jordens klipper ved atmosfære?
- Terningslanger har vist sig at bruge en række forskellige teknikker til mere effektivt at forfalske…


