Beregning af saltopløsningskoncentration:En trin-for-trin guide
Forstå problemet
* Oprindelig løsning: Kemikeren starter med 'm' gram saltvand, og en vis procentdel af den masse er salt.
* Ønsket løsning: Kemikeren ønsker at ende med en opløsning, der er dobbelt så salt (2 * original saltprocent).
* Mål: Bestem, hvor meget vand der skal tilsættes for at opnå dette.
Beregninger
1. Initial Salt Masse: Den oprindelige mængde salt i opløsningen er (procent/100) * m gm.
2. Ønsket saltmasse: For at have en opløsning dobbelt så salt, skal den endelige saltmasse være 2 * (procent/100) * m gm.
3. Saltmasseforskel: Forskellen i saltmasse mellem den indledende og endelige opløsning er (2 * (procent/100) * m gm) - ((procent/100) * m gm) =(procent/100) * m gm.
4. Vand tilføjet: Da mængden af salt forbliver konstant, repræsenterer forskellen i saltmasse mængden af vand, der skal tilsættes. Derfor skal du tilføje (procent/100) * m gm af vand.
Eksempel
Lad os sige, at kemikeren har 100 g saltvand, der er 5% salt.
* Indledende saltmasse:(5/100) * 100 gm =5 gm
* Ønsket saltmasse:2 * (5/100) * 100 gm =10 gm
* Saltmasseforskel:10 gm - 5 gm =5 gm
* Tilsat vand:5 g
Derfor skal kemikeren tilsætte 5 g vand for at gøre opløsningen 2 * 5 % =10 % salt.
Sidste artikelMolekyler vs. forbindelser:Forstå forskellen
Næste artikelForståelse af spontane redoxreaktioner:Betingelser og krav
 Varme artikler
Varme artikler
-
 Indfanger adfærden af enkeltatom-katalysatorer på fartenEn ny undersøgelse kontrollerede præcist fastgørelsen af platinatomer (hvide kugler) til en titaniumdioxidoverflade (gitterværk af røde og blå kugler). Den fandt, at deres positioner varierede fra a
Indfanger adfærden af enkeltatom-katalysatorer på fartenEn ny undersøgelse kontrollerede præcist fastgørelsen af platinatomer (hvide kugler) til en titaniumdioxidoverflade (gitterværk af røde og blå kugler). Den fandt, at deres positioner varierede fra a -
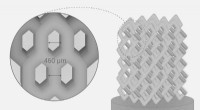 Forskere udviklede en ny metode til fremstilling af knogleimplantaterKnogleimplantat. Kredit:Pavel Odinev / Skoltech Forskere fra Skoltech Center for Design, Fremstilling, and Materials (CDMM) har udviklet en metode til at designe og fremstille kompleksformede kera
Forskere udviklede en ny metode til fremstilling af knogleimplantaterKnogleimplantat. Kredit:Pavel Odinev / Skoltech Forskere fra Skoltech Center for Design, Fremstilling, and Materials (CDMM) har udviklet en metode til at designe og fremstille kompleksformede kera -
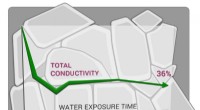 Forskere viser, at en lovende fast elektrolyt er hydrofobSkoltech-forskere og deres kolleger har vist, at LATP, en fast elektrolyt, der overvejes til brug i næste generations energilagring, er meget følsom over for vand, hvilket har direkte konsekvenser for
Forskere viser, at en lovende fast elektrolyt er hydrofobSkoltech-forskere og deres kolleger har vist, at LATP, en fast elektrolyt, der overvejes til brug i næste generations energilagring, er meget følsom over for vand, hvilket har direkte konsekvenser for -
 Rapid DNA identificerer ofre for undfangelsesbådbrandKredit:U.S. Department of Homeland Security 34 mennesker døde i en tragisk bådbrand den 2. september. 2019, ud for Santa Cruz Islands kyst, Californien. Fem besætningsmedlemmer slap med skader eft
Rapid DNA identificerer ofre for undfangelsesbådbrandKredit:U.S. Department of Homeland Security 34 mennesker døde i en tragisk bådbrand den 2. september. 2019, ud for Santa Cruz Islands kyst, Californien. Fem besætningsmedlemmer slap med skader eft
- Succesfuld syntese af en ny insulinanalog
- Hvilket materiale er sandsynligvis en isolator?
- Misinformation om fossilt brændstof kan sidestille en af de vigtigste klimaændringsrapporter, de…
- Lingvistiktimer for politiet kunne fange flere Dark Web-pædofile
- Hvad gør ilt og kuldioxid i kemisk forvitring?
- Rumteleskoper åbner gyldne spejlvinger en sidste gang på Jorden


