Beregning af opløsningsvarme:En trin-for-trin guide
Forstå begreberne
* Opløsningens varme: Den varme, der absorberes eller frigives, når et stof opløses i et opløsningsmiddel. En positiv opløsningsvarme indikerer en endoterm proces (varme absorberes), mens en negativ opløsningsvarme indikerer en eksoterm proces (varme frigives).
* Specifik varmekapacitet: Mængden af varme, der kræves for at hæve temperaturen på 1 gram af et stof med 1 grad Celsius. For vand er den specifikke varmekapacitet ca. 4.184 J/(g °C).
* Kalorimetri: Studiet af varmestrøm i kemiske og fysiske processer.
Beregninger
1. Beregn temperaturændringen:
ΔT =T2 - T1 =22,2 °C - 20,0 °C =2,2 °C
2. Beregn den varme, der absorberes af vandet:
q =m × c × ΔT
Hvor:
* q =varmeabsorberet (i joule)
* m =masse af vand (i gram) =1000,0 g
* c =specifik varmekapacitet for vand (i J/(g °C)) =4,184 J/(g °C)
* ΔT =temperaturændring (i °C) =2,2 °C
q =(1000,0 g) × (4,184 J/(g °C)) × (2,2 °C) =9184,8 J
Vigtige overvejelser:
* Forudsætninger: Vi antager, at den varme, der frigives af det opløselige barium, absorberes fuldstændigt af vandet. Dette er en tilnærmelse, da noget varme kan gå tabt til omgivelserne.
* Entalpiændring (ΔH): Opløsningsvarmen (q) er et mål for entalpiændringen (ΔH) af opløsningsprocessen. I dette tilfælde, da temperaturen af vandet steg, er opløsningsprocessen eksoterm (ΔH <0). Uden yderligere information kan vi dog ikke bestemme den nøjagtige værdi af ΔH.
Derfor er den omtrentlige varme, der absorberes af vandet på grund af opløsningen af barium, 9184,8 joule.
Vigtig bemærkning: Denne beregning giver kun en tilnærmelse af opløsningsvarmen. En mere præcis bestemmelse ville kræve et mere kontrolleret eksperiment, potentielt ved at bruge et kalorimeter for at minimere varmetabet til omgivelserne.
 Varme artikler
Varme artikler
-
 Biosensorteknologier til at tilbyde mere effektive tilgange til sygdomsbehandlingMonash Biomedicine Discovery Institutes professor Mibel Aguilar og Dr. John Lee ved siden af den nyudviklede biosensorteknologi. Kredit:Steve Morton Hver celle i vores kroppe er formet af dens y
Biosensorteknologier til at tilbyde mere effektive tilgange til sygdomsbehandlingMonash Biomedicine Discovery Institutes professor Mibel Aguilar og Dr. John Lee ved siden af den nyudviklede biosensorteknologi. Kredit:Steve Morton Hver celle i vores kroppe er formet af dens y -
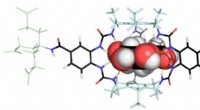 Glucosebindende molekyle kunne transformere behandlingen af diabetesReceptor bindende glucose. Kredit:University of Bristol Forskere fra University of Bristol har designet en ny syntetisk glukosebindende molekyleplatform, der bringer os et skridt tættere på udvikl
Glucosebindende molekyle kunne transformere behandlingen af diabetesReceptor bindende glucose. Kredit:University of Bristol Forskere fra University of Bristol har designet en ny syntetisk glukosebindende molekyleplatform, der bringer os et skridt tættere på udvikl -
 En teoretisk undersøgelse forklarer det naturlige udvalg af proteinerKunstnerisk repræsentation af sekvensudvælgelsen efter temperatur for et hydratiseret protein. Kredit:V. Bianco Forskere fra Institute of Nanoscience and Nanotechnology ved University of Barcelona
En teoretisk undersøgelse forklarer det naturlige udvalg af proteinerKunstnerisk repræsentation af sekvensudvælgelsen efter temperatur for et hydratiseret protein. Kredit:V. Bianco Forskere fra Institute of Nanoscience and Nanotechnology ved University of Barcelona -
 Enkeltkrystallinske kvaternære sulfid -nanobelterKobberbaserede kvaternære sulfid-nanomaterialer, især for Cu-Zn-In-S (CZIS) og Cu-Zn-Ga-S (CZGS), som består af giftfri elementer er attraktive kandidater til solfotokatalytisk brintproduktion på grun
Enkeltkrystallinske kvaternære sulfid -nanobelterKobberbaserede kvaternære sulfid-nanomaterialer, især for Cu-Zn-In-S (CZIS) og Cu-Zn-Ga-S (CZGS), som består af giftfri elementer er attraktive kandidater til solfotokatalytisk brintproduktion på grun
- Hvorfor er vinkelmomentum for et legeme lig med produktet dets øjeblik inerti og hastighed?
- Hvad er den dobbelte opviklede form af DNA?
- Sådan bestemmes køn af babyhjorte
- Hvilke to kræfter kan bremse genstande ned?
- Forskere introducerer et ratingsystem til at vurdere kvaliteten af evidens for politik
- Metallisk element Calcium kombineres med det ikke -metalliske ilt?


