Butenisomerer:Forståelse af C4H8 molekylære variationer
Den generelle formel for buten er C₄H₈ .
Her er de fire almindelige isomerer af buten:
* 1-buten: Dobbeltbindingen er i enden af kulstofkæden.
* cis-2-buten: Dobbeltbindingen er i midten af kulstofkæden, med begge hydrogenatomer på samme side.
* trans-2-buten: Dobbeltbindingen er i midten af kulstofkæden, med brinterne på modsatte sider.
* Isobuten (2-methylpropen): Kulstofkæden er forgrenet, med dobbeltbindingen for enden.
Du kan se disse strukturer illustreret i de fleste kemi lærebøger eller online ressourcer.
Sidste artikelEthan:Egenskaber og struktur af en simpel alkan
Næste artikelOvergangsmetaller i periode 5:Egenskaber og eksempler
 Varme artikler
Varme artikler
-
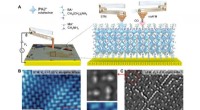 Ikke-invasiv billeddannelse af atomarrangement på sub-angstrom-skalaen i 2-D hybridperovskitterqPlus-baseret STM- og ncAFM-billeddannelse af RPP-overfladen. (A) Skema, der viser en kombineret STM- og ncAFM-billeddannelse af RPP-overfladen ved hjælp af en stemmegaffel-baseret qPlus-sensor. Atoml
Ikke-invasiv billeddannelse af atomarrangement på sub-angstrom-skalaen i 2-D hybridperovskitterqPlus-baseret STM- og ncAFM-billeddannelse af RPP-overfladen. (A) Skema, der viser en kombineret STM- og ncAFM-billeddannelse af RPP-overfladen ved hjælp af en stemmegaffel-baseret qPlus-sensor. Atoml -
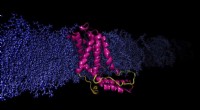 Undersøgelse afslører metodebegrænsninger til bestemmelse af proteinstrukturBeregningsmodel YidC2 protein indlejret cellemembran. Den modellerede sløjfe (gul), mangler i røntgenkrystalstrukturen, er afgørende for stabilisering af protein. Kredit:Sogol Moradi En ny undersø
Undersøgelse afslører metodebegrænsninger til bestemmelse af proteinstrukturBeregningsmodel YidC2 protein indlejret cellemembran. Den modellerede sløjfe (gul), mangler i røntgenkrystalstrukturen, er afgørende for stabilisering af protein. Kredit:Sogol Moradi En ny undersø -
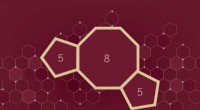 Gennembrudssyntesestrategi kan betyde bølge af nye medicinske forbindelserFSU-forskere har udtænkt en strategi til syntetisering af carbocykliske 5-8-5 smeltede ringsystemer, en molekylær struktur med potentielt bredt terapeutisk potentiale. Kredit:Benjamin Moten I farm
Gennembrudssyntesestrategi kan betyde bølge af nye medicinske forbindelserFSU-forskere har udtænkt en strategi til syntetisering af carbocykliske 5-8-5 smeltede ringsystemer, en molekylær struktur med potentielt bredt terapeutisk potentiale. Kredit:Benjamin Moten I farm -
 Bakterielle enzymer kapret til at skabe komplekse molekyler, der normalt fremstilles af planterKredit:CC0 Public Domain Kemikere ved Scripps Research har effektivt skabt tre familier af komplekse, oxygenholdige molekyler, der normalt kun kan opnås fra planter. Disse molekyler, kaldet terpe
Bakterielle enzymer kapret til at skabe komplekse molekyler, der normalt fremstilles af planterKredit:CC0 Public Domain Kemikere ved Scripps Research har effektivt skabt tre familier af komplekse, oxygenholdige molekyler, der normalt kun kan opnås fra planter. Disse molekyler, kaldet terpe
- Kan en første kvartal ocour under Toltal Solar Eclipse?
- Forskere udvikler syntetiske stilladser til at helbrede skadede sener og ledbånd
- Hvordan ansigt til ansigt stadig slår Facebook:Begrænsninger på størrelsen af vores offline so…
- Hvordan sexhandelstraumer påvirker den måde, dets overlevende forælder på
- Hvad er det mindst reaktive metal i orden?
- Studiet undersøger kommercielle hybrid-elektriske fly, reducerede kulstofemissioner


