Molekylær interaktion under væskeblanding:En detaljeret forklaring
1. Oprindelig tilstand:
* Før blanding: Molekylerne i hver væske er klynget sammen på grund af intermolekylære kræfter (som hydrogenbinding, dipol-dipol-interaktioner eller London-dispersionskræfter). De er i konstant tilfældig bevægelse inden for deres respektive faser.
2. Blandeproces:
* Diffusion: Når væskerne kommer i kontakt, begynder molekylerne ved grænsefladen at blande sig. Dette sker på grund af molekylers naturlige tendens til at sprede sig og optage ledig plads. Hver væskes molekyler diffunderer ind i den anden.
* Kollisioner: Molekylerne kolliderer konstant med hinanden. Disse kollisioner overfører energi, hvilket får nogle molekyler til at få energi og bevæge sig hurtigere, mens andre mister energi og bevæger sig langsommere.
* Blanding: Molekylerne i begge væsker bliver til sidst jævnt fordelt i hele blandingen. Dette sker på grund af den tilfældige bevægelse af molekyler og de konstante kollisioner, der får dem til at bevæge sig i alle retninger.
3. Ligevægt:
* Ensartet fordeling: Når væskerne er fuldt blandet, fordeles molekylerne ensartet i hele blandingen. Der er ikke længere adskilte områder af den ene eller den anden væske.
* Dynamisk ligevægt: Selvom molekylerne er jævnt fordelt, fortsætter de med at bevæge sig og støde sammen. Denne dynamiske ligevægt sikrer, at blandingen forbliver homogen over tid.
Faktorer, der påvirker blanding:
* Temperatur: Højere temperaturer fører til hurtigere molekylær bevægelse og derfor hurtigere blanding.
* Viskositet: Væsker med lavere viskositet blandes lettere, fordi deres molekyler kan bevæge sig mere frit.
* Opløselighed: I hvilket omfang væsker blandes afhænger af deres opløselighed. Nogle væsker er blandbare (fuldstændigt opløselige i hinanden), mens andre er ublandbare (må ikke blandes).
Vigtig bemærkning: Bevægelsen af molekyler i væsker er meget hurtig og tilfældig. Mens vi kan observere de makroskopiske virkninger af blanding (f.eks. dannelsen af en homogen opløsning), kan vi ikke direkte se de enkelte molekyler bevæge sig og kollidere.
 Varme artikler
Varme artikler
-
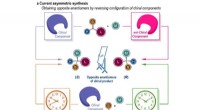 Forskere får adgang til begge enantiomerer efter varierende reaktionstidFigur 1. Strategier til opnåelse af begge enantiomerer af chirale molekyler. Kredit:SIOC Homokiralitet er et grundlæggende træk ved alle levende organismer. Det er velkendt, at et par enantiomerer
Forskere får adgang til begge enantiomerer efter varierende reaktionstidFigur 1. Strategier til opnåelse af begge enantiomerer af chirale molekyler. Kredit:SIOC Homokiralitet er et grundlæggende træk ved alle levende organismer. Det er velkendt, at et par enantiomerer -
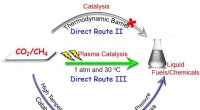 Gennembrud i direkte aktivering af CO2 og CH4 til flydende brændstoffer og kemikalierDirekte omdannelse af CO 2 og CH 4 til flydende brændstoffer. Kredit:University of Liverpool Forskere fra University of Liverpool har gjort et betydeligt gennembrud i den direkte omdannelse af
Gennembrud i direkte aktivering af CO2 og CH4 til flydende brændstoffer og kemikalierDirekte omdannelse af CO 2 og CH 4 til flydende brændstoffer. Kredit:University of Liverpool Forskere fra University of Liverpool har gjort et betydeligt gennembrud i den direkte omdannelse af -
 Variabel valens:Hvordan elementer ændrer deres ladningstilstande i kemiAf David Stewart • Opdateret 24. marts 2022 Elektroner kredser om en atomkerne i diskrete energiniveauer. De yderste elektroner - kendt som valenselektroner - bestemmer, hvordan et atom interagerer m
Variabel valens:Hvordan elementer ændrer deres ladningstilstande i kemiAf David Stewart • Opdateret 24. marts 2022 Elektroner kredser om en atomkerne i diskrete energiniveauer. De yderste elektroner - kendt som valenselektroner - bestemmer, hvordan et atom interagerer m -
 Opskalering af biohybride systemer til syntetisering af brændstoffer, kemikalierVisualisering af en bakteriecelle (øverst), der omdanner organiske molekylers kemiske energi til elektroner, der overføres til en uorganisk tinoxidkatalysator (nederst) via molekylære ledninger indlej
Opskalering af biohybride systemer til syntetisering af brændstoffer, kemikalierVisualisering af en bakteriecelle (øverst), der omdanner organiske molekylers kemiske energi til elektroner, der overføres til en uorganisk tinoxidkatalysator (nederst) via molekylære ledninger indlej
- Undersøgelse af forgiftningseffekten af kulstofaflejring under CO₂-elektroreduktion
- Hvordan vitaminvand virker
- Hvad overføres termisk energi mellem genstande, der har forskellig temperatur?
- Hvorfor sker der ingen brydning, når medierne har samme brydningsindeks?
- En hurtig nedadgående bevægelse af stenjord?
- Reagerer vismuthchlorid med natriumhydroxid?


