Svovlatomer i bariumsulfat (BaSO4):En trin-for-trin beregning
1. Forstå formlen
* BaSO4 repræsenterer bariumsulfat. Underskriften "4" efter oxygenet (O) angiver, at der er fire oxygenatomer i hvert molekyle af bariumsulfat.
* Det er vigtigt, at underskriften "1" er underforstået for barium (Ba) og svovl (S), hvilket betyder, at der er et atom af hvert i hvert molekyle.
2. Avogadros nummer
* Avogadros tal er 6.022 x 10²³ og repræsenterer antallet af partikler (atomer, molekyler osv.) i et mol af et stof.
3. Beregning
* Trin 1: Da der er et svovlatom pr. molekyle bariumsulfat, ved vi, at 0,45 mol BaSO4 indeholder 0,45 mol svovlatomer.
* Trin 2: For at finde antallet af svovlatomer skal du gange antallet af svovlatomer med Avogadros tal:
0,45 mol S × (6,022 x 10²³ atomer S / 1 mol S) =2,71 x 10²³ svovlatomer
Derfor er der ca. 2,71 x 10²³ svovlatomer i 0,45 mol BaSO4.
Sidste artikelChloridion (Cl⁻):Protoner og elektroner forklaret
Næste artikelKondensation:Forståelse af gas-til-væske-faseændringen
 Varme artikler
Varme artikler
-
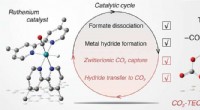 Overvågning af mellemprodukter i CO2 -omdannelse til formiat ved hjælp af metalkatalysatorTriethanolamin (TEOA) er aktivt engageret i centrale reaktionstrin i den fotokatalytiske cyklus til omdannelse af kuldioxid (CO2) af rutheniumcarbonylkomplekser. Kredit: Journal of the American Chemic
Overvågning af mellemprodukter i CO2 -omdannelse til formiat ved hjælp af metalkatalysatorTriethanolamin (TEOA) er aktivt engageret i centrale reaktionstrin i den fotokatalytiske cyklus til omdannelse af kuldioxid (CO2) af rutheniumcarbonylkomplekser. Kredit: Journal of the American Chemic -
 Forskere afslører robust ethan-fangende porøst organisk bur til effektiv anvendelse af ethylenrens…Kredit:Prof. YUANs gruppe Fjernelse af ethan (C 2 H 6 ) fra dets analoge ethylen (C 2 H 4 ) er af stor betydning i den petrokemiske industri, og er meget udfordrende på grund af deres lign
Forskere afslører robust ethan-fangende porøst organisk bur til effektiv anvendelse af ethylenrens…Kredit:Prof. YUANs gruppe Fjernelse af ethan (C 2 H 6 ) fra dets analoge ethylen (C 2 H 4 ) er af stor betydning i den petrokemiske industri, og er meget udfordrende på grund af deres lign -
 Forskere turbolader brintceller med ny ionledende copolymerMiguel Modestino, professor i kemisk og bimolekylær teknik (til højre) og ph.d. studerende Adlai Katzenberg, forfattet forskning, der beskriver en bemærkelsesværdig ny ionledende copolymer, der i høj
Forskere turbolader brintceller med ny ionledende copolymerMiguel Modestino, professor i kemisk og bimolekylær teknik (til højre) og ph.d. studerende Adlai Katzenberg, forfattet forskning, der beskriver en bemærkelsesværdig ny ionledende copolymer, der i høj -
 Forskere opdager superelastisk formhukommelsesmaterialeMaterialevidenskab og ingeniørprofessor Seok-Woo Lee og kolleger har opdaget superelastiske formhukommelsesegenskaber i et materiale, der kunne bruges under de hårdeste forhold, såsom det ydre rum. Kr
Forskere opdager superelastisk formhukommelsesmaterialeMaterialevidenskab og ingeniørprofessor Seok-Woo Lee og kolleger har opdaget superelastiske formhukommelsesegenskaber i et materiale, der kunne bruges under de hårdeste forhold, såsom det ydre rum. Kr
- Hvad er kraften i Newtons, der er nødvendig for at flytte et 1500 kg køretøj ved en acceleration …
- Hvor lille er for lille? Forskere finder ud af, at polarisering ændrer sig på nanoskala
- Den filippinske minister forbyder nye åbne miner til en værdi af $ 8 mia
- Når luft udøver en kraft kaldes den?
- Fejlsikker, rekonfigurerbare chips
- Hvilke bevægelser af solstof ligner dem, der koger i en gryde?


