Forståelse af iltstabilitet:Hvorfor O2 er mere stabil end O3
* Oxygen som et diatomisk molekyle (O2): Dette er den mest almindelige form for ilt, vi indånder. Det er meget stabilt, fordi de to oxygenatomer deler elektroner i en dobbeltbinding. Dette skaber en stærk binding og en fyldt ydre skal for hvert atom, hvilket gør det meget stabilt.
* Ozon (O3): Dette er et triatomisk molekyle med tre oxygenatomer. Det er *mindre* stabilt end oxygengas (O2) af et par grunde:
* Svagere obligationer: Bindingerne i ozon er svagere end dobbeltbindingerne i oxygengas. Det skyldes, at elektronerne er spredt ud over tre atomer i stedet for to.
* Resonansstrukturer: Ozons struktur kan repræsenteres af to resonansstrukturer, som bidrager til dens ustabilitet.
* Reaktivitet: Ozon er meget reaktivt og virker som et stærkt oxidationsmiddel. Denne reaktivitet er en konsekvens af dens ustabilitet.
Så hvorfor er diatomisk oxygen (O2) mere stabil end ozon (O3)?
Det kommer ned til styrken af de kemiske bindinger og stabiliteten af elektronkonfigurationen. Diatomisk oxygen har en stærk dobbeltbinding og en fyldt ydre skal, hvilket gør den meget stabil. Ozon er med dets svagere bindinger og resonansstrukturer mindre stabilt og mere reaktivt.
 Varme artikler
Varme artikler
-
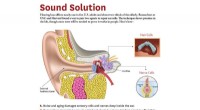 Tilslutning af hørehjælpemolekyler til øreknoglenKredit:USC Forskere ved USC og Harvard har udviklet en ny tilgang til at reparere celler dybt inde i øret - et potentielt middel, der kan genoprette hørelsen for millioner af ældre mennesker og an
Tilslutning af hørehjælpemolekyler til øreknoglenKredit:USC Forskere ved USC og Harvard har udviklet en ny tilgang til at reparere celler dybt inde i øret - et potentielt middel, der kan genoprette hørelsen for millioner af ældre mennesker og an -
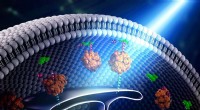 Bygger broer inden i cellen - ved hjælp af lysProteiner er byggestenene i broen mellem organeller i cellen. Kredit:Yun Huang og Yubin Zhou Hver celle i kroppen består af et antal små forseglede membranøse underenheder kaldet organeller, og de
Bygger broer inden i cellen - ved hjælp af lysProteiner er byggestenene i broen mellem organeller i cellen. Kredit:Yun Huang og Yubin Zhou Hver celle i kroppen består af et antal små forseglede membranøse underenheder kaldet organeller, og de -
 Bedre metaloxider til at booste de grønne legitimationsoplysninger for mange energiapplikationerNærbillede af metaloxiderne. Kredit:Imperial College London Forskere har løst en vigtig hindring i grønnere fremstilling, kulstofopsamling, energilagring og gasrensning - ved hjælp af metaloxider.
Bedre metaloxider til at booste de grønne legitimationsoplysninger for mange energiapplikationerNærbillede af metaloxiderne. Kredit:Imperial College London Forskere har løst en vigtig hindring i grønnere fremstilling, kulstofopsamling, energilagring og gasrensning - ved hjælp af metaloxider. -
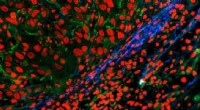 Oplyser vævsdannelse gennem flourescensBillede af tumorgrænse taget ved hjælp af fluorescensmikroskopi. Det nye markørmolekyle viser grænsen for tumoren i blåt; tumorvævet kan ses over det til venstre. Grøn:kollagen, rød:cellekerner. Kredi
Oplyser vævsdannelse gennem flourescensBillede af tumorgrænse taget ved hjælp af fluorescensmikroskopi. Det nye markørmolekyle viser grænsen for tumoren i blåt; tumorvævet kan ses over det til venstre. Grøn:kollagen, rød:cellekerner. Kredi
- Hvis to objekter bevægede sig mod hinanden med halvdelen af lysets hastighed, bevæger de sig rel…
- En celle er en kompleks samling af arbejdsdele?
- Hvilken overførsel af varme i atmosfæren ved opadgående bevægelsesluft?
- De største skovbrande i amerikansk historie efter areal:En omfattende oversigt
- Sådan ser du levende maskiner
- Punkteringsmekanikken blev endelig forklaret


