Forståelse af opløselighed:Hvorfor stoffer opløses
1. Intermolekylære kræfter:
* Interaktioner mellem opløsningsmiddel og opløsning: Opløsningsmiddelmolekylerne skal have en stærk tiltrækning til de opløste molekyler. Denne tiltrækning er baseret på intermolekylære kræfter som hydrogenbinding, dipol-dipol-interaktioner eller London-spredningskræfter.
* Opløsnings-opløsningsinteraktioner: De opløste molekyler skal kunne bryde væk fra hinanden. Hvis de opløste molekyler er for stærkt tiltrukket af hinanden, vil de ikke være i stand til at opløses.
2. Polaritet:
* Like opløses som: Dette er et almindeligt ordsprog i kemi. Polære opløsningsmidler (som vand) har en tendens til at opløse polære opløste stoffer (som sukker), mens ikke-polære opløsningsmidler (som olie) har tendens til at opløse upolære opløste stoffer (som fedt).
3. Entropi:
* Øget lidelse: Når et opløst stof opløses, bliver det mere spredt i opløsningsmidlet, hvilket fører til en stigning i entropi (uorden) af systemet. Denne stigning i entropi favoriserer opløsningsprocessen.
4. Temperatur:
* Højere temperaturer favoriserer generelt opløsning: Øget temperatur giver mere energi til at overvinde de intermolekylære kræfter, der holder det opløste stof sammen og tillader opløsningsmiddelmolekylerne at bevæge sig hurtigere, hvilket øger interaktioner med det opløste stof.
5. Tryk:
* Tryk påvirker primært opløsningen af gasser i væsker: Øget tryk tvinger flere gasmolekyler i opløsning. Dette er grunden til, at kuldioxid opløses bedre i sodavand under højere tryk.
Eksempel:
* Sukker opløses i vand: Sukker er et polært molekyle, og vand er et polært opløsningsmiddel. Hydrogenbindingen mellem vandmolekyler og hydroxylgrupperne i sukker giver stærke interaktioner mellem opløsningsmiddel og opløst stof. Sukkermolekylerne har også nok energi til at bryde fra hinanden, så de kan omgives af vandmolekyler og opløses.
Opsummering:
Et stof kan opløses i et andet stof, hvis opløsningsmiddelmolekylerne har en stærk tiltrækning til de opløste molekyler, de opløste molekyler kan bryde fra hinanden, og den samlede proces fører til en stigning i entropien. Polariteten af opløsningsmidlet og det opløste stof samt temperatur og tryk spiller også vigtige roller.
Sidste artikelVolume Occupied by 1 Gram:A Guide for Different Substances
Næste artikelFlydende ilttransport:udfordringer og alternativer
 Varme artikler
Varme artikler
-
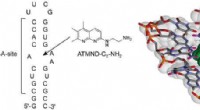 Den tætteste ikke-aminoglykosidligand til det bakterielle ribosomale RNA A-stedKemisk struktur af ATMND-C 2 -NH 2 og sekvensen af den bakterielle (Escherichia coli) A-sted-holdige RNA-model anvendt i denne undersøgelse. Det viser også den mulige struktur af komplekset mell
Den tætteste ikke-aminoglykosidligand til det bakterielle ribosomale RNA A-stedKemisk struktur af ATMND-C 2 -NH 2 og sekvensen af den bakterielle (Escherichia coli) A-sted-holdige RNA-model anvendt i denne undersøgelse. Det viser også den mulige struktur af komplekset mell -
 Forskere skaber ny form for dyrket kødKredit:Pixabay/CC0 Public Domain McMaster-forskere har udviklet en ny form for dyrket kød ved hjælp af en metode, der lover mere naturlig smag og tekstur end andre alternativer til traditionelt kø
Forskere skaber ny form for dyrket kødKredit:Pixabay/CC0 Public Domain McMaster-forskere har udviklet en ny form for dyrket kød ved hjælp af en metode, der lover mere naturlig smag og tekstur end andre alternativer til traditionelt kø -
 Emballage lavet af bananplanter et alternativ til a-peelingKredit:CC0 Public Domain Biologisk nedbrydelige plastik poser lavet af bananplanter lyder lidt...bananer, men et par UNSW-forskere har fundet en måde at gøre det på, og det kunne løse to industria
Emballage lavet af bananplanter et alternativ til a-peelingKredit:CC0 Public Domain Biologisk nedbrydelige plastik poser lavet af bananplanter lyder lidt...bananer, men et par UNSW-forskere har fundet en måde at gøre det på, og det kunne løse to industria -
 Undersøgelse opdaterer etnobotanik, fytokemi og farmakologisk undersøgelse af slægten Didymocarpu…Kredit:Consolata Nanjala Slægten Didymorcapus Wall. omfatter mere end 100 arter, der er vidt udbredt fra Himalaya til den malaysiske halvø. Arter i denne slægt er blevet brugt i traditionel medicin
Undersøgelse opdaterer etnobotanik, fytokemi og farmakologisk undersøgelse af slægten Didymocarpu…Kredit:Consolata Nanjala Slægten Didymorcapus Wall. omfatter mere end 100 arter, der er vidt udbredt fra Himalaya til den malaysiske halvø. Arter i denne slægt er blevet brugt i traditionel medicin
- Hvad ville der ske, hvis en erosion ikke forekom i klippecyklussen?
- Du har stadig ikke brug for et ægte ID. Deadline skubbet tilbage til 2023
- Lille paragliding bille, der levede med dinosaurer opdaget i rav, ved navn Jason
- Selvsamlende nanopartikler kunne forbedre MR-scanning til kræftdiagnose
- Høje isklipper kan udløse store kælvningsbegivenheder - og hurtig havniveaustigning
- Hvilken evolutionær kraft reducerer den genetiske mangfoldighed af en befolkning ved at øge lignen…


