Elektrisk ledningsevne af materialer:bindinger og fast tilstand
Materialer, der leder elektricitet i fast tilstand:
* Metallige bindinger: Disse er dannet af et "hav" af delokaliserede elektroner, der frit kan bevæge sig gennem metallets struktur. Denne frie bevægelse af elektroner giver mulighed for fremragende elektrisk ledningsevne. Eksempler:Kobber, guld, sølv, aluminium.
* Nogle kovalente forbindelser: Mens kovalente bindinger generelt involverer delte elektroner, har visse kovalente forbindelser elektroner, der holdes relativt løst og kan bevæge sig inden for krystalstrukturen. Disse materialer kaldes halvledere, og deres ledningsevne kan påvirkes af temperatur eller urenheder. Eksempler:Silicium, germanium.
Materialer, der kun leder elektricitet, når de er smeltet eller opløst i vand:
* Ioniske forbindelser: Ionbindinger dannes af den elektrostatiske tiltrækning mellem positivt og negativt ladede ioner. I fast tilstand holdes disse ioner i et stift gitter og kan ikke bevæge sig frit. Men når ionerne smeltes eller opløses i vand, bliver de mobile og kan føre elektrisk strøm. Eksempler:Natriumchlorid (NaCl), kaliumbromid (KBr).
Nøglepunkter:
* Fri elektronbevægelse: Elektrisk ledningsevne afhænger grundlæggende af ladede partiklers (elektroner eller ioner) evne til at bevæge sig frit.
* Binding og ledningsevne: Typen af kemisk binding bestemmer mobiliteten af disse ladede partikler.
* Halvledere: Disse materialer fungerer som en bro mellem ledere og isolatorer. Deres ledningsevne kan styres af eksterne faktorer.
Lad mig vide, hvis du har flere spørgsmål om ledningsevne eller limning!
 Varme artikler
Varme artikler
-
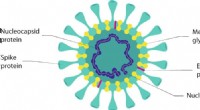 Antivirale overflader, overfladebelægninger og deres virkningsmekanismerFig. 1:Skematisk over en virusstruktur baseret på coronavirus. Kredit: Kommunikationsmaterialer (2021). DOI:10.1038/s43246-021-00153-y Forskere fra The National Physical Laboratory (NPL) og Natio
Antivirale overflader, overfladebelægninger og deres virkningsmekanismerFig. 1:Skematisk over en virusstruktur baseret på coronavirus. Kredit: Kommunikationsmaterialer (2021). DOI:10.1038/s43246-021-00153-y Forskere fra The National Physical Laboratory (NPL) og Natio -
 Forskere opdager vejen til at forbedre spilskiftende batterielektrodeElbilproducenter er intenst interesserede i lithium-rige batterikatoder, der kan øge rækkevidden betydeligt. En ny undersøgelse åbner en vej til at få dem til at leve op til deres løfte. Kredit:Stanfo
Forskere opdager vejen til at forbedre spilskiftende batterielektrodeElbilproducenter er intenst interesserede i lithium-rige batterikatoder, der kan øge rækkevidden betydeligt. En ny undersøgelse åbner en vej til at få dem til at leve op til deres løfte. Kredit:Stanfo -
 Aktiv maskinlæring til opdagelse og krystallisering af gigantiske polyoxometalatmolekylerKredit:Wiley Hvem er den bedre eksperimenterende, et menneske eller en robot? Når det kommer til at udforske syntetiske og krystallisationsbetingelser for uorganiske gigantiske molekyler, aktivt l
Aktiv maskinlæring til opdagelse og krystallisering af gigantiske polyoxometalatmolekylerKredit:Wiley Hvem er den bedre eksperimenterende, et menneske eller en robot? Når det kommer til at udforske syntetiske og krystallisationsbetingelser for uorganiske gigantiske molekyler, aktivt l -
 Ny metode til mere præcis bestemmelse af dødstidspunkt på gerningsstederKredit:CC0 Public Domain Forskere fra Amsterdam UMC, universitetet i Amsterdam og det nederlandske retsmedicinske institut (NFI) - partnere i den retsmedicinske forskningsinstitution Co van Ledden
Ny metode til mere præcis bestemmelse af dødstidspunkt på gerningsstederKredit:CC0 Public Domain Forskere fra Amsterdam UMC, universitetet i Amsterdam og det nederlandske retsmedicinske institut (NFI) - partnere i den retsmedicinske forskningsinstitution Co van Ledden
- Hvad er det nødvendigt at give levende ting energi?
- Hvorfor er jod fast, men andre halogener er gasser?
- Målinger af acceleration gives i enheder af?
- Hvad synker ikke i vand, fordi dens densitet er mindre end vand?
- Du var ikke den eneste, der streamede flere videoer i 2019 - det gjorde hele verden
- Airbnb siger tvunget til at annullere bookinger i henhold til ny japansk lov


