Ionisk ledningsevne:Hvordan og hvorfor ioniske forbindelser leder elektricitet
* Solid State: I deres faste tilstand har ioniske forbindelser en stiv, krystallinsk struktur. Ionerne holdes fast i en fast position af stærke elektrostatiske kræfter. Dette forhindrer den frie bevægelse af ladede partikler, så de ikke kan lede elektricitet.
* Opløst eller smeltet tilstand: Når de opløses i vand eller smeltes, brydes ionbindingerne, og ionerne bliver frie til at bevæge sig. Dette skaber en mobil pool af ladede partikler, der kan bære en elektrisk strøm. Bevægelsen af disse ioner giver mulighed for strømning af elektricitet.
Opsummering:
* Fast ioniske forbindelser: Led ikke elektricitet.
* Opløste eller smeltede ioniske forbindelser: Led elektricitet.
Eksempel: Bordsalt (NaCl) er en ionisk forbindelse. Det leder ikke elektricitet i sin faste form, men det leder elektricitet, når det er opløst i vand eller smeltet.
 Varme artikler
Varme artikler
-
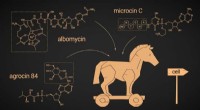 Pas på andre bakterier, der bærer gaver:Forskning præsenterer nye potentielle antimikrobielle mid…Trojansk hest-strategi Kredit:Pavel Odinev/Skoltech Skoltech -forskere undersøgte de antibiotiske forbindelser, der anvender en trojansk hest -strategi for at komme ind i en bakteriecelle uigenken
Pas på andre bakterier, der bærer gaver:Forskning præsenterer nye potentielle antimikrobielle mid…Trojansk hest-strategi Kredit:Pavel Odinev/Skoltech Skoltech -forskere undersøgte de antibiotiske forbindelser, der anvender en trojansk hest -strategi for at komme ind i en bakteriecelle uigenken -
 Forståelse af kemisk ligevægt:principper, typer og indflydelsesfaktorerRomoloTavani/iStock/GettyImages I hverdagen beskriver ligevægt kroppens balancesans. Inden for kemi refererer kemisk ligevægt til en tilstand, hvor koncentrationerne af reaktanter og produkter forbli
Forståelse af kemisk ligevægt:principper, typer og indflydelsesfaktorerRomoloTavani/iStock/GettyImages I hverdagen beskriver ligevægt kroppens balancesans. Inden for kemi refererer kemisk ligevægt til en tilstand, hvor koncentrationerne af reaktanter og produkter forbli -
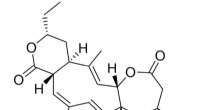 Et usædvanligt molekyle beskytter nerveceller mod degenerationDen kemiske struktur af collinolacton. Kredit:University of Tübingen Et internationalt forskerhold ledet af professor Stephanie Grond fra Institute of Organic Chemistry ved University of Tübingen
Et usædvanligt molekyle beskytter nerveceller mod degenerationDen kemiske struktur af collinolacton. Kredit:University of Tübingen Et internationalt forskerhold ledet af professor Stephanie Grond fra Institute of Organic Chemistry ved University of Tübingen -
 Undersøgelse viser, at keramik kan deformere som metaller, hvis det sintres under et elektrisk feltPurdue-forskere observerede for første gang, hvordan keramik dannet under et elektrisk felt overraskende ændrer form i stedet for at gå i stykker, når det komprimeres ved høj belastning. På billedet:U
Undersøgelse viser, at keramik kan deformere som metaller, hvis det sintres under et elektrisk feltPurdue-forskere observerede for første gang, hvordan keramik dannet under et elektrisk felt overraskende ændrer form i stedet for at gå i stykker, når det komprimeres ved høj belastning. På billedet:U
- Hvorfor er solen det vigtigste objekt i universet?
- Hvor ofte ser folk en Saturn -himmel?
- Føler du dig selvtilfreds med dit solcelletag? Ikke så hurtigt
- Risiko i forsyningskæder er forskellig efter branche, ny rapport finder
- Antiferromagnetisk dysprosium afslører magnetisk omskiftning med mindre energi
- Hvad er den nordlige stjerne?


