Forståelse af kemisk ligevægt:principper, typer og indflydelsesfaktorer
RomoloTavani/iStock/GettyImages
I hverdagen beskriver ligevægt kroppens balancesans. Inden for kemi refererer kemisk ligevægt til en tilstand, hvor koncentrationerne af reaktanter og produkter forbliver konstante over tid, selvom de fremadrettede og omvendte reaktioner fortsætter med at forekomme med lige store hastigheder.
Lov om kemisk ligevægt
Loven om kemisk ligevægt, ofte udtrykt via ligevægtskonstanten (K), siger, at for en reaktion ved konstant temperatur og tryk forbliver forholdet mellem produktkoncentrationerne og reaktantkoncentrationerne (hver hævet til deres støkiometriske koefficienter) uændret.
Begrebet kemisk ligevægt
Overvej en reversibel reaktion:
A + B <=> C + D
Efterhånden som reaktionen skrider frem, stiger koncentrationerne af C og D, mens A og B falder. Til sidst udlignes de fremadgående og omvendte reaktionshastigheder, og koncentrationerne plateau. Denne dynamiske balance er kendetegnende for kemisk ligevægt.
Typer af kemisk ligevægt
Ligevægte kan klassificeres i:
- Homogen – reaktanter og produkter ligger i samme fase.
- Heterogen – reaktanter og produkter optager forskellige faser.
Betingelser for ligevægt
For at et system kan nå ligevægt, skal følgende holdes:
- Alle målbare egenskaber (koncentration, tryk, farve osv.) forbliver konstante ved en fast temperatur.
- Systemet kan opnå ligevægt fra enten fremadgående eller tilbagegående retning.
- En katalysator kan accelerere tilgangen til ligevægt, men ændrer ikke dens position.
- Ligevægten er i sagens natur dynamisk.
Faktorer, der ændrer ligevægt
Le Chateliers princip forudsiger, hvordan et system reagerer på forstyrrelser:
- Koncentrationsændringer – Tilsætning af reaktant driver reaktionen fremad; tilføjelse af produkt fører det tilbage.
- Temperatur – Forøgelse af temperaturen favoriserer den endoterme retning; sænkning af temperaturen favoriserer den eksoterme retning.
- Tryk – Stigende tryk (faldende volumen) flytter ligevægten mod siden med færre gasmolekyler.
- Katalysatorer – Fremskynd begge retninger lige meget, hvilket forkorter tiden til at nå ligevægt.
- Inerte gasser – Ved konstant volumen har de ingen effekt; ved konstant tryk kan de påvirke det samlede tryk.
 Varme artikler
Varme artikler
-
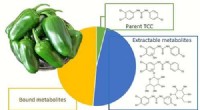 Peberplante suger antibiotika til personlig plejeproduktKredit:American Chemical Society Det kan nogle gange være svært at finde tandpasta, sæber og andre toiletartikler uden antibiotika. Deres popularitet har forårsaget en stigning i miljøniveauer af
Peberplante suger antibiotika til personlig plejeproduktKredit:American Chemical Society Det kan nogle gange være svært at finde tandpasta, sæber og andre toiletartikler uden antibiotika. Deres popularitet har forårsaget en stigning i miljøniveauer af -
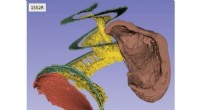 Enestående 3D-billeder af menneskets øres anatomi til genoprettelse af hørelsenBillede af det indre øre. Kredit:Canadian Light Source Ved at bruge avancerede teknikker ved den canadiske lyskilde (CLS) ved University of Saskatchewan, forskere har skabt tredimensionelle billed
Enestående 3D-billeder af menneskets øres anatomi til genoprettelse af hørelsenBillede af det indre øre. Kredit:Canadian Light Source Ved at bruge avancerede teknikker ved den canadiske lyskilde (CLS) ved University of Saskatchewan, forskere har skabt tredimensionelle billed -
 Proteinmissil øger muligheden for sygdomsgennembrudKredit:University of Dundee University of Dundee forskere har vist, at det er muligt hurtigt at målrette og ødelægge specifikke proteiner i celler, øger muligheden for at udvikle nye måder at målr
Proteinmissil øger muligheden for sygdomsgennembrudKredit:University of Dundee University of Dundee forskere har vist, at det er muligt hurtigt at målrette og ødelægge specifikke proteiner i celler, øger muligheden for at udvikle nye måder at målr -
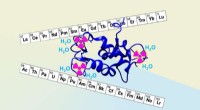 Gå ud over Moder Naturs molekyler for at målrette radioaktive metallerDet naturlige protein lanmodulin (afbildet i marineblåt) blev biokonstrueret af et samarbejde mellem forskere fra LLNL og Penn State University for bedre at opfange og adskille elementer fundet i nukl
Gå ud over Moder Naturs molekyler for at målrette radioaktive metallerDet naturlige protein lanmodulin (afbildet i marineblåt) blev biokonstrueret af et samarbejde mellem forskere fra LLNL og Penn State University for bedre at opfange og adskille elementer fundet i nukl
- Mikrober, der lever uafhængigt, men samarbejder og deler næringsstoffer, hvad det kaldes?
- Bluetooth-signaler fra din smartphone kan automatisere Covid-19-kontaktsporing og samtidig bevare pr…
- Hvilke er mennesker, der betragtes som?
- Et system afgiver 196 kj varme til omgivelserne og gør 4,20 x 10 2 arbejde på Hvad er ændring i d…
- Er det, hvad der ikke direkte gør det muligt for fotosyntesen at finde sted i et blad?
- Hvad er nettobevægelsen af elektriske ladninger i en enkelt retning?


