Beregning af det samlede antal elektroner for ethvert molekyle eller ion
Af bidragende skribent • Opdateret 30. august 2022
Atomer binder ved at dele elektroner, og at kende elektrontallet i en forbindelse er det første skridt til at forstå dens kemi. Ved hjælp af det periodiske system og grundlæggende aritmetik kan du bestemme, hvor mange elektroner der er til stede i ethvert molekyle eller ion.
Trin 1:Identificer elementerne og deres mængder
Skriv hvert grundstof i den kemiske formel ned, og noter, hvor mange atomer der forekommer af hvert. For eksempel:
- KNO3 – Kalium (1 atom), nitrogen (1 atom), ilt (3 atomer)
- SO4 2- – Svovl (1 atom), ilt (4 atomer)
Trin 2:Hent atomnumre
Se et pålideligt periodisk system (f.eks. PubChem periodiske system ) for at finde hvert elements atomnummer - det helt tal direkte over dets symbol. I eksemplerne ovenfor:K=19, N=7, O=8, S=16.
Trin 3:Beregn elektronsummen
Multiplicer hvert elements atomnummer med dets atomantal, og tilføj derefter produkterne:
- KNO3 :(19×1)+(7×1)+(8×3)=50 elektroner
- SO4 2- :(16×1)+(8×4)=48 elektroner (før ladningsjustering)
Trin 4:Juster for ionisk opladning
For ioner skal du ændre totalen fra trin 3 med ladningsværdien:Tilføj ladningen for negative ioner, træk fra for positive ioner, og lad den være uændret for neutrale arter. Sulfat-ionen bærer en 2-ladning, så 48+2=50 elektroner.
Værktøjer, du skal bruge
- Videnskabelig lommeregner (eller regneark)
- Adgang til en ajourført periodisk tabel
Referencer
- Whitten, K.W.; Davis, R.E.; Peck, L.; Stanley, G.G. Kemi , 2009.
 Varme artikler
Varme artikler
-
 Mastering Moles in Chemistry:En praktisk guide til molar masse og støkiometriAf Judy Tyler | Opdateret 30. august 2022 I kemi, en muldvarp er den grundlæggende enhed, der forbinder antallet af partikler til massen i støkiometriske ligninger. Et mol af ethvert stof indeholder
Mastering Moles in Chemistry:En praktisk guide til molar masse og støkiometriAf Judy Tyler | Opdateret 30. august 2022 I kemi, en muldvarp er den grundlæggende enhed, der forbinder antallet af partikler til massen i støkiometriske ligninger. Et mol af ethvert stof indeholder -
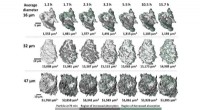 Cementerer fremtidenBilleddannelse af udviklingen af tre cementpartikler. Grøn indikerer opløste mineraler, hulrum og mineralske forbindelser med lav masse. Mørkegrå indikerer solide materialer. Billeddannelsen indiker
Cementerer fremtidenBilleddannelse af udviklingen af tre cementpartikler. Grøn indikerer opløste mineraler, hulrum og mineralske forbindelser med lav masse. Mørkegrå indikerer solide materialer. Billeddannelsen indiker -
 Lægemiddel mod superbakterier fundet i kråbærEt urinkateter belagt med antimikrobielle peptider forhindrer alvorlige urinvejsinfektioner. Docent Anna Maria Pirttilä og CEO Mysore Tejesvi fra Chain Antimicrobials Oy er personerne bag peptidinnova
Lægemiddel mod superbakterier fundet i kråbærEt urinkateter belagt med antimikrobielle peptider forhindrer alvorlige urinvejsinfektioner. Docent Anna Maria Pirttilä og CEO Mysore Tejesvi fra Chain Antimicrobials Oy er personerne bag peptidinnova -
 Vandbehandling - ny metode eliminerer hormonerMetoden udviklet af KIT kombinerer fordelene ved at binde mikroforurenende stoffer med aktivt kul med fordelene ved ultrafiltrering. Kredit:Sandra Göttisheim, SÆT Hormoner og andre mikroforurenend
Vandbehandling - ny metode eliminerer hormonerMetoden udviklet af KIT kombinerer fordelene ved at binde mikroforurenende stoffer med aktivt kul med fordelene ved ultrafiltrering. Kredit:Sandra Göttisheim, SÆT Hormoner og andre mikroforurenend
- Hvorfor vises forskellige stjerner i sæsoner?
- Hubble tager et nærbillede af kometen NEOWISE
- Hvad er meningen med at give gaver? En antropolog forklarer, at denne ældgamle del er menneske
- Hvad er en almindelig hindring, som enhver civilisation skal stå over for Wikipedia?
- Hvordan ændrer erosion og afsætning overfladen?
- Hvordan definerer du bedst en videnskabelig lov?


