Elektrisk ledningsevne af ioniske og kovalente forbindelser:Tilstandsafhængighed
Ioniske forbindelser
* Solid State: Gør ikke lede elektricitet. Ionerne holdes tæt i et krystalgitter og kan ikke bevæge sig frit.
* Flydende tilstand (smeltet) :Opførsel elektricitet. Når ionerne er smeltet, er de frie til at bevæge sig og bære den elektriske strøm.
* Vandig opløsning: Adfærd elektricitet. Når ionerne er opløst i vand, dissocieres og bliver mobile, hvilket giver mulighed for elektrisk ledning.
Kovalente forbindelser
* Solid State: De fleste gør ikke lede elektricitet. Kovalente forbindelser deler elektroner, og disse elektroner er typisk lokaliseret i bindingerne, ikke frie til at bevæge sig.
* Flydende tilstand: De fleste gør ikke lede elektricitet. I lighed med den faste tilstand er elektronerne stadig for det meste lokaliseret i bindingerne.
* Vandig opløsning: Nogle gør leder elektricitet, men kun hvis de er polære og ionisere i vand. Dette skyldes, at ioniseringsprocessen skaber ioner, der så kan føre strømmen. For eksempel opløses saltsyre (HCl) i vand og danner H+ og Cl-ioner, hvilket gør den ledende.
Opsummering:
* Ioniske forbindelser leder elektricitet i deres smeltede tilstand og i vandige opløsninger .
* Kovalente forbindelser leder generelt ikke elektricitet, bortset fra polære kovalente forbindelser, der ioniserer i vand.
Bemærk: Der er nogle undtagelser fra disse generelle regler. For eksempel er grafit, en form for kulstof, en kovalent forbindelse, der kan lede elektricitet i sin faste tilstand på grund af sin unikke struktur.
 Varme artikler
Varme artikler
-
 Ingeniører gør mikrofluidik modulopbygget ved hjælp af de populære sammenlåsende blokkeMIT -forskere har udviklet en ny platform for mikrofluidik, ved hjælp af LEGO klodser. Vist her, væske strømmer gennem bittesmå kanaler fræset ind i sidevæggene på LEGO klodser. Kredit:Massachusetts I
Ingeniører gør mikrofluidik modulopbygget ved hjælp af de populære sammenlåsende blokkeMIT -forskere har udviklet en ny platform for mikrofluidik, ved hjælp af LEGO klodser. Vist her, væske strømmer gennem bittesmå kanaler fræset ind i sidevæggene på LEGO klodser. Kredit:Massachusetts I -
 Fremstilling af lysaktiverede proteinerRaziye Karapinar (til venstre) og Stefan Herlitze Kredit:RUB, Kramer En ny strategi til design af lysfølsomme proteiner er blevet udviklet af forskere ved Ruhr-Universität Bochum (RUB). Sådanne pr
Fremstilling af lysaktiverede proteinerRaziye Karapinar (til venstre) og Stefan Herlitze Kredit:RUB, Kramer En ny strategi til design af lysfølsomme proteiner er blevet udviklet af forskere ved Ruhr-Universität Bochum (RUB). Sådanne pr -
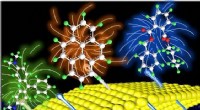 Ny Raman-metode fanger målmolekyler i små huller aktivtSkematisk diagram af princippet om den generelle overfladeforstærkede Raman-spektroskopimetode til aktivt at fange målmolekyler i små huller med opløsningsmidlet. Kredit:GE Meihong For nylig, Prof
Ny Raman-metode fanger målmolekyler i små huller aktivtSkematisk diagram af princippet om den generelle overfladeforstærkede Raman-spektroskopimetode til aktivt at fange målmolekyler i små huller med opløsningsmidlet. Kredit:GE Meihong For nylig, Prof -
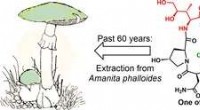 Syntetiserer et dødeligt svampetoksinKredit:American Chemical Society Dødskapssvampen har en lang historie som et redskab til mord og selvmord, går tilbage til oldtidens romertid. Svampen, Amanita phalloides , producerer et af verd
Syntetiserer et dødeligt svampetoksinKredit:American Chemical Society Dødskapssvampen har en lang historie som et redskab til mord og selvmord, går tilbage til oldtidens romertid. Svampen, Amanita phalloides , producerer et af verd
- Når en 20 Newton -kasse løftes 5 meter ud af gulvet, hvor meget joules fungerer det?
- Repræsenterer et fritkroppsdiagram kræfter, der virker på systemet?
- Hvad er der i både en dyrecelle og en plantecelle?
- Virkningen af virksomheders sociale ansvar på brandsalg
- Hvorfor anses energi fra vand, der flyder i floden, for at være en indirekte form af solenergi?
- Hvad er sammensætningen af afslørende middel to tone opløsning alfa plak?


