Ioniske forbindelser:Elektrisk ledningsevne i faste og smeltede tilstande
Her er hvorfor:
* Ioniske forbindelser: Disse forbindelser dannes af den elektrostatiske tiltrækning mellem positivt ladede ioner (kationer) og negativt ladede ioner (anioner).
* Solid State: I fast tilstand holdes ionerne stift i en krystalgitterstruktur. Dette faste arrangement forhindrer den frie bevægelse af ioner, og derfor ingen elektrisk ledningsevne.
* Smeltet tilstand: Når ionerne smeltes, bryder ionerne fri fra gitterstrukturen og bliver mobile. Dette giver dem mulighed for at bære elektrisk ladning, hvilket resulterer i ledningsevne.
Eksempel: Natriumchlorid (NaCl) er en almindelig ionisk forbindelse. Det leder ikke elektricitet i sin faste form (bordsalt), men leder godt, når det smelter.
 Varme artikler
Varme artikler
-
 Forbedring af varmegenanvendelse med termodiffusionseffektenKredit:CC0 Public Domain Absorptionsvarme transformatorer kan effektivt genbruge spildvarmen, der genereres i forskellige industrier. I disse enheder, specialiserede væsker danner tynde film, når
Forbedring af varmegenanvendelse med termodiffusionseffektenKredit:CC0 Public Domain Absorptionsvarme transformatorer kan effektivt genbruge spildvarmen, der genereres i forskellige industrier. I disse enheder, specialiserede væsker danner tynde film, når -
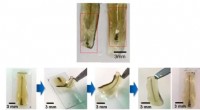 Grænseflade med hjernenNervesystemet er fyldt med kodet information:tanker, følelser, motorstyring. Dette system i vores kroppe er en gåde, og jo mere vi kan gøre for at forstå det, jo mere kan vi gøre for at forbedre menne
Grænseflade med hjernenNervesystemet er fyldt med kodet information:tanker, følelser, motorstyring. Dette system i vores kroppe er en gåde, og jo mere vi kan gøre for at forstå det, jo mere kan vi gøre for at forbedre menne -
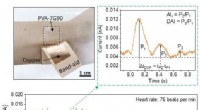 Opfindelsen tilbyder en ny mulighed for overvågning af hjertesundhedEt team fra Purdue University udviklede selvdrevne bærbare triboelektriske nanogeneratorer med polyvinylalkohol-baserede kontaktlag til overvågning af kardiovaskulær sundhed. Kredit:Wenzhuo Wu/Purdue
Opfindelsen tilbyder en ny mulighed for overvågning af hjertesundhedEt team fra Purdue University udviklede selvdrevne bærbare triboelektriske nanogeneratorer med polyvinylalkohol-baserede kontaktlag til overvågning af kardiovaskulær sundhed. Kredit:Wenzhuo Wu/Purdue -
 Forståelse af de to kernekomponenter i et atom:Nucleus og Electron CloudHemera Technologies/PhotoObjects.net/Getty Images Atomer er stoffets grundlæggende byggesten, der definerer det synlige univers. Hvert atom er sammensat af to væsentlige komponenter:kernen og den omg
Forståelse af de to kernekomponenter i et atom:Nucleus og Electron CloudHemera Technologies/PhotoObjects.net/Getty Images Atomer er stoffets grundlæggende byggesten, der definerer det synlige univers. Hvert atom er sammensat af to væsentlige komponenter:kernen og den omg
- Hvilken tid på året kan du se din Zodiac -konstellation?
- Hvor lang tid tager det for rumfærgen at få måne?
- Flere skovelefantbestande tæt på at kollapse i Centralafrika
- I vandkraftværker omdannes energien fra bevægende vand til elektrisk strøm. Hvilken slags transfo…
- Hvordan kan du se månen, når den er så langt væk?
- Kystrisici og arealudnyttelsespolitik skaber økonomiske afvejninger for at ruste Oregon-kysten


