Ionisk ledningsevne:Forståelse af elektrisk adfærd i faste og smeltede tilstande
Ioniske forbindelser:En påmindelse
* Struktur: Ioniske forbindelser dannes af den elektrostatiske tiltrækning mellem positivt ladede ioner (kationer) og negativt ladede ioner (anioner). De danner en stiv, krystallinsk gitterstruktur.
* Elektroner: Elektroner i ioniske forbindelser er tæt bundet til ionerne og kan ikke bevæge sig frit.
Hvorfor faste stoffer ikke leder
* Faste positioner: I fast tilstand er ioner låst i en fast gitterstruktur. De er ude af stand til at bevæge sig frit.
* Ingen afgiftsudbydere: Da elektronerne er bundet til ionerne, er der ingen frie ladningsbærere til at føre en elektrisk strøm.
Hvorfor Molten State opfører sig
* Mobilitet: Når en ionforbindelse smelter, svækkes de stærke elektrostatiske kræfter, der holder ionerne sammen. Ionerne bliver mobile og kan bevæge sig frit.
* Tillægsudbydere: De mobile ioner, der bærer deres positive eller negative ladninger, fungerer som ladningsbærere. Når et elektrisk potentiale påføres, bevæger disse ioner sig mod den modsat ladede elektrode, hvilket skaber en elektrisk strøm.
Analogi
Forestil dig et fyldt rum fyldt med mennesker (ioner), som alle er tæt pakket og ikke kan bevæge sig (solid state). Forestil dig nu, at de samme mennesker alle bevæger sig frit rundt (smeltet tilstand). Hvis du ønsker at få en besked på tværs af lokalet, er det meget nemmere at gøre det, når folk bevæger sig rundt!
Nøgleudtag: Elektrisk ledningsevne i ioniske stoffer er afhængig af ionernes mobilitet. I fast tilstand er de fikserede, mens de i smeltet tilstand er frie til at bevæge sig og bære ladning.
 Varme artikler
Varme artikler
-
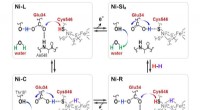 Mikroorganismer bygger de bedste brændstofeffektive brintcellerProtoner overføres mellem det aktive NiFe-sted og det omgivende protein gennem Cyt546- og Glu34-resterne under den katalytiske reaktion af [NiFe]-hydrogenase. Kredit:Shun Hirota For alle de fremsk
Mikroorganismer bygger de bedste brændstofeffektive brintcellerProtoner overføres mellem det aktive NiFe-sted og det omgivende protein gennem Cyt546- og Glu34-resterne under den katalytiske reaktion af [NiFe]-hydrogenase. Kredit:Shun Hirota For alle de fremsk -
 Visualisering af varmeflow i bambus kan hjælpe med at designe mere energieffektive og brandsikre by…Kredit:Pixabay Modificerede naturlige materialer vil være en væsentlig komponent i en bæredygtig fremtid, men først er der behov for en detaljeret forståelse af deres egenskaber. Måden varme strøm
Visualisering af varmeflow i bambus kan hjælpe med at designe mere energieffektive og brandsikre by…Kredit:Pixabay Modificerede naturlige materialer vil være en væsentlig komponent i en bæredygtig fremtid, men først er der behov for en detaljeret forståelse af deres egenskaber. Måden varme strøm -
 Ny metode åbner vejen for skærende værktøjer med længere levetidKostas Sarakinos, Davide Sangiovanni og Georgio Almyras. Kredit:Anna Nilsen Forskere ved Linköpings Universitet, LiU, har udviklet en teoretisk model, der muliggør simuleringer for at vise, hvad d
Ny metode åbner vejen for skærende værktøjer med længere levetidKostas Sarakinos, Davide Sangiovanni og Georgio Almyras. Kredit:Anna Nilsen Forskere ved Linköpings Universitet, LiU, har udviklet en teoretisk model, der muliggør simuleringer for at vise, hvad d -
 Automatisk databaseoprettelse til materialeopdagelse:Innovation fra frustrationAutogenerering af en ultraviolet-synlig (UV-vis) absorptionsspektral database via en dobbelt eksperimentel og beregningsmæssig kemisk datavej ved hjælp af ALCFs Theta-supercomputer. Kredit:Jacqueline
Automatisk databaseoprettelse til materialeopdagelse:Innovation fra frustrationAutogenerering af en ultraviolet-synlig (UV-vis) absorptionsspektral database via en dobbelt eksperimentel og beregningsmæssig kemisk datavej ved hjælp af ALCFs Theta-supercomputer. Kredit:Jacqueline
- En mulig forklaring på, hvorfor der ikke er fundet sorte huller i mellemstørrelse
- Hjernen, hvordan din fungerer
- Hvilke celler skal opbevare energi fra biologiske membraner og kemiske budbringere?
- Fælles elementer i kulhydrater og vand:en kemisk sammenligning
- Hvad ligner et stykke sten, der ligner det materiale, der er dannet til planeter?
- Hvor er det mest volumen på i jordlagene?


