Beregning af pH af en bufferopløsning (HNO₂ &NaNO₂)
Forståelse af kemien
* HNO₂ er en svag syre: Det ioniserer kun delvist i opløsning.
* NaNO₂ er saltet af dets konjugerede base: Det giver nitrit-ionen (NO2⁻), som er den konjugerede base af HNO2.
* Tilstedeværelsen af både den svage syre og dens konjugerede base skaber en bufferopløsning: Denne opløsning modstår ændringer i pH.
Henderson-Hasselbalch-ligningen
Vi bruger Henderson-Hasselbalch-ligningen til at beregne pH-værdien af denne bufferopløsning:
pH =pKa + log([konjugatbase]/[syre])
1. Find pKa af HNO₂:
* pKa af salpetersyrling (HNO2) er ca. 3,14. Du kan finde denne værdi i en tabel med syredissociationskonstanter (Ka-værdier).
2. Tilslut koncentrationerne:
* [syre] =[HNO2] =0,16 M
* [konjugeret base] =[NO2⁻] =0,50 M
3. Beregn pH:
pH =3,14 + log(0,50 / 0,16)
pH =3,14 + log(3,125)
pH ≈ 3,14 + 0,49
pH ≈ 3,63
Derfor er opløsningens pH ca. 3,63.
 Varme artikler
Varme artikler
-
 Enhedsopdatering muliggør mobiltest for vira, bakterier og aktive toksinerSandia National Laboratories kemiker Chung-Yan Koh, venstre, og tidligere Sandia bioingeniør Chris Phaneuf, ret, behold den nyligt opdaterede SpinDx diagnostiske enhed. Kredit:Jules Bernstein Du s
Enhedsopdatering muliggør mobiltest for vira, bakterier og aktive toksinerSandia National Laboratories kemiker Chung-Yan Koh, venstre, og tidligere Sandia bioingeniør Chris Phaneuf, ret, behold den nyligt opdaterede SpinDx diagnostiske enhed. Kredit:Jules Bernstein Du s -
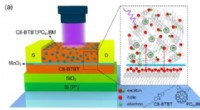 Forskere udvikler ultrafølsomme organiske fototransistorer baseret på en ny hybridlagsarkitekturStrukturen af hybrid-lag fototransistor. Kredit:LI Jia Organiske fototransistorer (OPTer) er meget udbredt i miljø-/sundhedsovervågning, kvantekommunikation, kemisk/biomedicinsk sansning, fjernb
Forskere udvikler ultrafølsomme organiske fototransistorer baseret på en ny hybridlagsarkitekturStrukturen af hybrid-lag fototransistor. Kredit:LI Jia Organiske fototransistorer (OPTer) er meget udbredt i miljø-/sundhedsovervågning, kvantekommunikation, kemisk/biomedicinsk sansning, fjernb -
 Termoelementer:Anvendelser, hvordan de fungerer og nøgleanvendelserAf Kim Lewis Opdateret 24. marts 2022 Termoelementer er temperatursensorer, der er lavet af to metallegeringer. Når de to metaller bringes sammen for at danne et kryds, genereres en spænding, når d
Termoelementer:Anvendelser, hvordan de fungerer og nøgleanvendelserAf Kim Lewis Opdateret 24. marts 2022 Termoelementer er temperatursensorer, der er lavet af to metallegeringer. Når de to metaller bringes sammen for at danne et kryds, genereres en spænding, når d -
 Forskere har fundet en måde at skabe lægemiddelmolekyler ud fra kulilteResultaterne af atomeffektivitetsreaktioner. Kredit:Denis Chusov Forskere fra RUDN Universitet har i samarbejde med russiske og udenlandske kolleger studeret reduktive amineringsreaktioner. De nye
Forskere har fundet en måde at skabe lægemiddelmolekyler ud fra kulilteResultaterne af atomeffektivitetsreaktioner. Kredit:Denis Chusov Forskere fra RUDN Universitet har i samarbejde med russiske og udenlandske kolleger studeret reduktive amineringsreaktioner. De nye


