Forudsigelse af produkter af enkelte erstatningsreaktioner:Jern og kobber(II)nitrat
Forstå enkeltudskiftningsreaktioner
Enkeltudskiftningsreaktioner involverer et element, der erstatter et andet i en forbindelse. Den generelle form er:
A + BC → AC + B
Anvendelse af principperne på vores reaktion
1. Identificer det mere reaktive metal: Jern (Fe) er mere reaktivt end kobber (Cu) baseret på aktivitetsrækken af metaller. Dette betyder, at jern kan fortrænge kobber fra dets forbindelse.
2. Skriv den balancerede ligning:
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
Produkter:
Produkterne af reaktionen er:
* Jern(II)nitrat (Fe(NO₃)₂): Jernet erstatter kobberet i nitratforbindelsen.
* Kobber (Cu): Det fortrængte kobbermetal er dannet som et fast stof.
Nøglepunkter
* Aktivitetsserie: Aktivitetsrækken af metaller hjælper med at bestemme, om en enkelt erstatningsreaktion vil forekomme. Et metal højere på serien kan forskyde et metal lavere på serien.
* Balancering: Sørg for at afbalancere den kemiske ligning for at sikre det samme antal atomer af hvert grundstof på begge sider af ligningen.
Sidste artikelJern(II) Nitrat Farve:Egenskaber og udseende
Næste artikelBegrænsningsreaktantberegning:Natriumkarbonat og calciumchlorid
 Varme artikler
Varme artikler
-
 Organiske metalskeletter lavet til at fungere som væskerEn udfordring for holdet var at få en krystallinsk MOF til at opføre sig som en porøs væske. Holdet opdagede, hvordan man modificerer overfladen af relativt store MOF-nanopartikler med passende kemi
Organiske metalskeletter lavet til at fungere som væskerEn udfordring for holdet var at få en krystallinsk MOF til at opføre sig som en porøs væske. Holdet opdagede, hvordan man modificerer overfladen af relativt store MOF-nanopartikler med passende kemi -
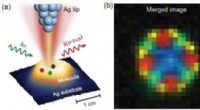 Scanning Raman picoscopy:En ny metode til bestemmelse af molekylær kemisk struktur(a) Skematisk scanning af Raman pikoskopi (SRP). Når en laserstråle fokuseres ind i nanorummet mellem den atomistisk skarpe spids og substratet, et meget stærkt og meget lokaliseret plasmonisk felt vi
Scanning Raman picoscopy:En ny metode til bestemmelse af molekylær kemisk struktur(a) Skematisk scanning af Raman pikoskopi (SRP). Når en laserstråle fokuseres ind i nanorummet mellem den atomistisk skarpe spids og substratet, et meget stærkt og meget lokaliseret plasmonisk felt vi -
 Hæmatitbaserede nanotrådsstrukturer for at forbedre sol-til-brændstofkonvertering i fotoelektroke…Et materiale til brug i fotoelektrokemisk vandspaltning, der ikke kun er billigere end eksisterende alternativer, men øger både effektiviteten og outputtet af processen. Kredit:ICN2 ICN2-forskere
Hæmatitbaserede nanotrådsstrukturer for at forbedre sol-til-brændstofkonvertering i fotoelektroke…Et materiale til brug i fotoelektrokemisk vandspaltning, der ikke kun er billigere end eksisterende alternativer, men øger både effektiviteten og outputtet af processen. Kredit:ICN2 ICN2-forskere -
 Proteinkæder, der selv dannes til spiralformede fletningerSEM-mikrofotografier af fletningstopologier observeret i geler af 2. a, Tegneseriediagrammer, der viser tostrengede sammenfiltringer og deres tilsvarende flettede ord. Fletningsordet beskriver mønster
Proteinkæder, der selv dannes til spiralformede fletningerSEM-mikrofotografier af fletningstopologier observeret i geler af 2. a, Tegneseriediagrammer, der viser tostrengede sammenfiltringer og deres tilsvarende flettede ord. Fletningsordet beskriver mønster
- Hvilken side af Mars vender mod solen?
- Hvilket udtryk beskriver ned faldne blokke af skorpe afgrænset af stejlt dypning af normale fejl?
- Hvad er udtrykket for gas produceret af aerosoler og fremstilling, der ødelægger jordens ozonlag?
- Trifluoreddikesyre virker som trifluormethyleringsmiddel i aren CH-funktionalisering
- Hvilken energikilde er blevet brugt længst?
- Hvad er fordelen ved at bruge en sol stadig?


