Begrænsningsreaktantberegning:Natriumkarbonat og calciumchlorid
1. Skriv den afbalancerede kemiske ligning:
Na₂CO3(aq) + CaCl2•2H2O(aq) → CaCO3(s) + 2NaCl(aq) + 2H2O(l)
2. Beregn molarmasserne:
* Na2CO3:(2 * 22,99) + 12,01 + (3 * 16,00) =105,99 g/mol
* CaCl2•2H2O:40,08 + (2 * 35,45) + (2 * 18,02) =147,02 g/mol
3. Konverter masse til mol:
* Mol Na₂CO₃:1,00 g / 105,99 g/mol =0,00943 mol
* Mol CaCl2•2H2O:1,00 g / 147,02 g/mol =0,00680 mol
4. Bestem den begrænsende reaktant:
* Brug af molforholdet fra den balancerede ligning: Ligningen viser et 1:1 molforhold mellem Na2CO3 og CaCl2•2H2O.
* Sammenlign muldvarpe: Da vi har færre mol CaCl2•2H2O (0,00680 mol) end Na2CO3 (0,00943 mol), er CaCl2•2H2O den begrænsende reaktant.
Forklaring:
Den begrænsende reaktant er den, der bliver fuldstændigt forbrugt først, hvilket forhindrer reaktionen i at fortsætte videre. I dette tilfælde vil reaktionen stoppe, selvom vi har flere mol Na₂CO3, når alt CaCl2•2H2O er brugt op.
 Varme artikler
Varme artikler
-
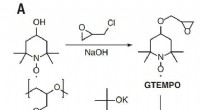 Forskere viser den højeste rapporterede ledningsevne for organisk radikal polymerDen monomersyntese og ringåbningspolymerisationsbaserede syntetiske skema, der bruges til at generere PTEO-radikalpolymeren. Kredit: Videnskab (2018). DOI:10.1126/science.aao7287 Et team af forsk
Forskere viser den højeste rapporterede ledningsevne for organisk radikal polymerDen monomersyntese og ringåbningspolymerisationsbaserede syntetiske skema, der bruges til at generere PTEO-radikalpolymeren. Kredit: Videnskab (2018). DOI:10.1126/science.aao7287 Et team af forsk -
 Fødevaresikkerhed:Bestråling og æteriske oliedampe til behandling af kornINRS professor Monique Lacroix er ekspert i videnskaber anvendt på fødevarer, såsom bestråling. Kredit:Christian Fleury (INRS) En kombineret behandling af bestråling og æteriske oliedampe kunne ef
Fødevaresikkerhed:Bestråling og æteriske oliedampe til behandling af kornINRS professor Monique Lacroix er ekspert i videnskaber anvendt på fødevarer, såsom bestråling. Kredit:Christian Fleury (INRS) En kombineret behandling af bestråling og æteriske oliedampe kunne ef -
 Hurtig 3D-print med synligt lysDette komplekse objekt blev 3D-printet på omkring 2,5 timer ved hjælp af synligt lys. Kredit:Tilpasset fra ACS Central Science 2020, DOI:10.1021/acscentsci.0c00929 3-D-print har drevet innovatio
Hurtig 3D-print med synligt lysDette komplekse objekt blev 3D-printet på omkring 2,5 timer ved hjælp af synligt lys. Kredit:Tilpasset fra ACS Central Science 2020, DOI:10.1021/acscentsci.0c00929 3-D-print har drevet innovatio -
 Dykker ned i atomområdetAtomer, molekyler og bindingerne, der holder dem sammen – jeg vil gerne se disse ting, som de faktisk optræder i naturen, siger Wilson Ho, UCI’s Donald Bren professor i fysik og astronomi og kemi, her
Dykker ned i atomområdetAtomer, molekyler og bindingerne, der holder dem sammen – jeg vil gerne se disse ting, som de faktisk optræder i naturen, siger Wilson Ho, UCI’s Donald Bren professor i fysik og astronomi og kemi, her
- Hvorfor fremstiller kroppen urin?
- Antimalariamedicin tilbyder et smørbord af nye herbicider
- Forudsigelighed af tidsmæssige netværk kvantificeret ved en entropi-rate-baseret ramme
- Dopant giver graphene solceller den højeste effektivitet endnu
- Sådan fungerer efterforskning af gerningssted
- Hvorfor måles temperaturen ved -273K?


