Beregning af iltproduktion ved nedbrydning af kaliumchlorat
1. Afbalanceret kemisk ligning:
Reaktionen for nedbrydning af kaliumchlorat (KClO3) er:
2 KClO3 → 2 KCl + 3 O2
2. Moleforhold:
Ud fra den afbalancerede ligning ser vi, at 2 mol KClO₃ producerer 3 mol O₂.
3. Beregn mol O₂:
* Brug molforholdet til at finde mol produceret O₂:
(5,00 x 10⁻2 mol KClO3) * (3 mol O2 / 2 mol KClO3) =7,50 x 10⁻2 mol O2
4. Konverter mol til volumen (forudsat STP):
* Ved standard temperatur og tryk (STP) fylder 1 mol af enhver gas 22,4 l.
* Beregn volumen af O₂:
(7,50 x 10⁻² mol O2) * (22,4 L/mol) =1,68 L O2
Derfor kan 5,00 x 10⁻² mol KClO₃ producere 1,68 L O₂ ved STP.
Sidste artikelZinkoxid (ZnO) Atomsammensætning:Forståelse af formlen
Næste artikelFarve på [Ni(NH3)6]2+:Forståelse af den gule komplekse ion
 Varme artikler
Varme artikler
-
 Sort plastik kan ikke genbruges - men vi har lige fundet en måde at bruge kulstoffet i vedvarende e…Kredit:Goskova Tatiana/Shutterstock Det store problem med plastik er, at selvom de holder i meget lang tid, de fleste smides ud efter kun én brug. Siden plastik blev opfundet i 1950erne, omkring 8
Sort plastik kan ikke genbruges - men vi har lige fundet en måde at bruge kulstoffet i vedvarende e…Kredit:Goskova Tatiana/Shutterstock Det store problem med plastik er, at selvom de holder i meget lang tid, de fleste smides ud efter kun én brug. Siden plastik blev opfundet i 1950erne, omkring 8 -
 Papirkurv til skat:Forskere konverterer kommunalt affald til biobrændstofforstadierBerkeley Lab-forskerne Ning Sun (til venstre) og Jipeng Yan, medforfattere til en ny undersøgelse om konvertering af affald til biobrændstofprækursorer, hos Advanced Biofuels and Bioproducts Process D
Papirkurv til skat:Forskere konverterer kommunalt affald til biobrændstofforstadierBerkeley Lab-forskerne Ning Sun (til venstre) og Jipeng Yan, medforfattere til en ny undersøgelse om konvertering af affald til biobrændstofprækursorer, hos Advanced Biofuels and Bioproducts Process D -
 For brintkraft, verdslige materialer kan være næsten lige så gode som dyr platinForskere brugte plasma til at skabe nye katalysatorer, der er meget billigere end og næsten lige så effektive som standard, platin-gruppe versioner. Kredit:Princeton University Som alle, der har k
For brintkraft, verdslige materialer kan være næsten lige så gode som dyr platinForskere brugte plasma til at skabe nye katalysatorer, der er meget billigere end og næsten lige så effektive som standard, platin-gruppe versioner. Kredit:Princeton University Som alle, der har k -
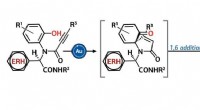 Kemiker udvikler syntesemetode for 28 biologisk aktive molekylerKredit:RUDN Universitet RUDN Universitetskemiker Erik Van der Eycken har fundet frem til en ny metode til syntese af en stor gruppe komplekse poly-heterocykliske organiske forbindelser, som kan ha
Kemiker udvikler syntesemetode for 28 biologisk aktive molekylerKredit:RUDN Universitet RUDN Universitetskemiker Erik Van der Eycken har fundet frem til en ny metode til syntese af en stor gruppe komplekse poly-heterocykliske organiske forbindelser, som kan ha
- Forskere skal lære robotter at skelne mellem sandwich-ingredienser
- Er jorden fra regnskoven god eller dårlig?
- Giv en grund til, at kedlen mister mindre varme end gryde ved ledningsprocessen?
- Lysshow over amerikansk himmel sandsynligvis SpaceX-affald på vej ind i atmosfæren igen
- Ubæredygtig arktisk skibsfart risikerer at accelerere skaderne på det arktiske miljø
- Hvad er 3 produkter af et brændende stearinlys?


