Blykloridsyntese:Forståelse af reaktionen med natrium og nitrat
* Temne er ikke involveret: De reaktanter, du har angivet, er natrium (Na) og nitrat (NO₃⁻). Der er ingen bly (Pb) til stede.
* Nitrat er en polyatomisk ion: Nitrat (NO₃⁻) er en negativt ladet ion og kan ikke eksistere alene. Det skal parres med en positivt ladet ion for at danne en neutral forbindelse.
* Natriumnitrat er en stabil forbindelse: Natrium og nitrat vil reagere og danne natriumnitrat (NaNO₃), en stabil forbindelse.
For at fremstille blychlorid (PbCl₂) skal du reagere en blyforbindelse med en chloridforbindelse. For eksempel:
Reaktion:
Bly(II)nitrat (Pb(NO₃)₂) + Natriumchlorid (NaCl) → Blychlorid (PbCl₂) + Natriumnitrat (NaNO₃)
Balanceret ligning:
Pb(NO3)₂(aq) + 2NaCl(aq) → PbCl2(s) + 2NaNO3(aq)
Forklaring:
* Reaktionen frembringer et bundfald af blychlorid (PbCl₂), fordi det er uopløseligt i vand.
* Koefficienterne foran hver forbindelse sikrer, at antallet af atomer i hvert grundstof er ens på begge sider af ligningen.
 Varme artikler
Varme artikler
-
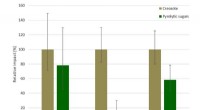 Bæredygtighed af nyt creosotalternativ bekræftetKredit:BTG Biomass Technology Group En nylig offentliggjort undersøgelse har bekræftet bæredygtighedsoplysningerne for et nyt biobaseret alternativ til creosot, der er ved at blive udviklet i Bio4
Bæredygtighed af nyt creosotalternativ bekræftetKredit:BTG Biomass Technology Group En nylig offentliggjort undersøgelse har bekræftet bæredygtighedsoplysningerne for et nyt biobaseret alternativ til creosot, der er ved at blive udviklet i Bio4 -
 Ny proces fremmer området for kulstofudnyttelseFeng Jiao, lektor i kemisk og biomolekylær teknik ved University of Delaware, er førende inden for kulstofopsamling og -udnyttelse. Kredit:Joy Smoker I et forsøg på at udvikle bæredygtige løsninge
Ny proces fremmer området for kulstofudnyttelseFeng Jiao, lektor i kemisk og biomolekylær teknik ved University of Delaware, er førende inden for kulstofopsamling og -udnyttelse. Kredit:Joy Smoker I et forsøg på at udvikle bæredygtige løsninge -
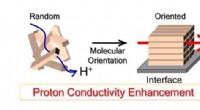 Få mere kontrol over brændselscellemembranerMolekylær orientering forbedrer protonkonduktion i protonkonduktive polymerer. Kredit:Yuki Nagao Mere organisering på molekylært niveau kan forbedre effektiviteten af membraner, der bruges i bri
Få mere kontrol over brændselscellemembranerMolekylær orientering forbedrer protonkonduktion i protonkonduktive polymerer. Kredit:Yuki Nagao Mere organisering på molekylært niveau kan forbedre effektiviteten af membraner, der bruges i bri -
 Forbedring af genleveringsmetoderKredit:Royal Society of Chemistry Forskere i Kina undersøger nye måder at behandle kræft på ved hjælp af genterapi. Vi finder ud af, hvordan deres arbejde inspirerede dette smukke og indviklede de
Forbedring af genleveringsmetoderKredit:Royal Society of Chemistry Forskere i Kina undersøger nye måder at behandle kræft på ved hjælp af genterapi. Vi finder ud af, hvordan deres arbejde inspirerede dette smukke og indviklede de
- Montering af en firkantet pind i et rundt hul - den overraskende struktur af uran bundet i hæmatit
- Hvem er den første person, der opdager eksistensen af farve i lys?
- Hvad er hydroxidionkoncentrationen i en vandig opløsning, som hydronium 0,13M?
- Er et fersketræ monocot eller dicot?
- Billede:Udskåret visning af nanopartikler i en neural celle
- Fremstilling af et gennemsigtigt fleksibelt materiale af silke og nanorør


