Energioverførsel i kemiske reaktioner:Endoterm vs. eksoterm
* Energiinput (endotermiske reaktioner): Nogle reaktioner kræver energi for at fortsætte. Denne energi absorberes fra omgivelserne, hvilket får temperaturen til at falde. Eksempler omfatter smeltende is eller fotosyntese.
* Energioutput (eksotermiske reaktioner): Andre reaktioner frigiver energi til omgivelserne, hvilket får temperaturen til at stige. Eksempler omfatter afbrænding af træ eller en forbrændingsreaktion.
Ud over energi involverer kemiske reaktioner også overførsel af:
* Elektroner: Dette er grundlæggende for de fleste kemiske reaktioner. Elektroner overføres mellem atomer, ændrer deres kemiske bindinger og danner nye stoffer. Dette kan ske gennem:
* Ionisk binding: Fuldstændig overførsel af elektroner mellem atomer, hvilket skaber ioner med modsatte ladninger.
* Kovalent binding: Deling af elektroner mellem atomer, dannelse af molekyler.
* Atomer: Selvom det ikke altid er synligt, involverer nogle reaktioner omlejring af atomer i molekyler. Dette kan føre til dannelse af nye forbindelser.
Nøgleudtag: Alle kemiske reaktioner involverer overførsel af energi og ofte overførsel af elektroner og/eller atomer. Type og mængde af overførsel dikterer reaktionens karakteristika.
 Varme artikler
Varme artikler
-
 Bygge broer med vandmolekylerVandmolekyler danner komplekse strukturer på en jernoxidoverflade. Kredit:Vienna University of Technology Et hold ved TU Wien har nu beviset bag spekulationerne om, at vandmolekyler kan danne komp
Bygge broer med vandmolekylerVandmolekyler danner komplekse strukturer på en jernoxidoverflade. Kredit:Vienna University of Technology Et hold ved TU Wien har nu beviset bag spekulationerne om, at vandmolekyler kan danne komp -
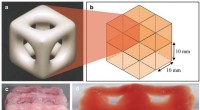 3-D-print skaber superbløde strukturer, der kopierer hjerne og lungerStruktur af en enkelt enhed; hvordan otte enheder passer sammen; to visninger af en trykt og fast struktur med otte enheder. Kredit:Imperial College London En ny 3D-printteknik gør det muligt for
3-D-print skaber superbløde strukturer, der kopierer hjerne og lungerStruktur af en enkelt enhed; hvordan otte enheder passer sammen; to visninger af en trykt og fast struktur med otte enheder. Kredit:Imperial College London En ny 3D-printteknik gør det muligt for -
 En strømlinet tilgang til bestemmelse af termiske egenskaber for krystallinske faste stoffer og leg…Et neuralt netværk, der bærer fuld krystal -symmetri, muliggør effektiv træning af krystallinske faste stoffer. Kredit:Massachusetts Institute of Technology I et essay i september 2020 i Naturene
En strømlinet tilgang til bestemmelse af termiske egenskaber for krystallinske faste stoffer og leg…Et neuralt netværk, der bærer fuld krystal -symmetri, muliggør effektiv træning af krystallinske faste stoffer. Kredit:Massachusetts Institute of Technology I et essay i september 2020 i Naturene -
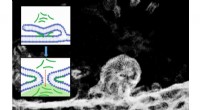 Hvordan trænger peptider ind i celler? To sider af samme møntElektronmikroskopibillede af en todelt cellemembran og det tilsvarende molekylære skema for processen. Kredit:@ IOCB Prag Den simple transport af lægemidler direkte ind i cellerne er et af de prim
Hvordan trænger peptider ind i celler? To sider af samme møntElektronmikroskopibillede af en todelt cellemembran og det tilsvarende molekylære skema for processen. Kredit:@ IOCB Prag Den simple transport af lægemidler direkte ind i cellerne er et af de prim
- IceBridge lancerer to sæt antarktiske flyvninger
- Hvor lang tid tager det lys at rejse fra den ene side af den anden side af galaksen?
- Hvordan trafiksignaler favoriserer biler og modvirker at gå
- GM afskediger omkring 4, 000 funktionærer:kilde
- Kan tyngdekraften lig med nul?
- Cellulær respiration frigiver energi ved at nedbryde glukose i nærvær af kuldioxid?


