Neutronkonservering i kemiske reaktioner:En detaljeret forklaring
Her er hvorfor:
* Neutroner er en del af kernen i et atom. De bidrager til atomets masse.
* Kemiske reaktioner involverer omlejring af atomer, ikke skabelse eller ødelæggelse af dem. Atomer er simpelthen omarrangeret til forskellige molekyler.
* Antallet af neutroner i hvert atom forbliver konstant under en kemisk reaktion.
Derfor skal det samlede antal neutroner bevares.
Eksempel:
Overvej reaktionen mellem hydrogengas (H2) og oxygengas (O2) for at danne vand (H2O):
2H2 + O2 -> 2H20
* Reaktanter:
* 2 brintmolekyler (4 brintatomer)
* 1 oxygenmolekyle (2 oxygenatomer)
* Produkter:
* 2 vandmolekyler (4 brintatomer og 2 oxygenatomer)
Hvis vi antager, at brint- og oxygenatomerne har de mest almindelige isotoper (hydrogen-1 og oxygen-16), så:
* Reaktanter: 4 neutroner (fra brintatomerne) + 32 neutroner (fra oxygenatomerne) =36 neutroner
* Produkter: 4 neutroner (fra brintatomerne) + 32 neutroner (fra oxygenatomerne) =36 neutroner
Som du kan se, er antallet af neutroner det samme i både reaktanterne og produkterne.
Bemærk: Mens antallet af neutroner forbliver konstant, kan antallet af protoner ændre sig i nukleare reaktioner (reaktioner, der involverer kernen af et atom). I nukleare reaktioner er massen ikke strengt bevaret, og det samlede antal neutroner i reaktanterne er muligvis ikke lig med det samlede antal neutroner i produkterne.
Sidste artikelForståelse af hydroxylgruppen (OH) i organisk kemi
Næste artikelBeregn molekyler fra muldvarpe:En trin-for-trin guide
 Varme artikler
Varme artikler
-
 At tælle alkanisomerer:en praktisk vejledningAf Kevin Beck | Opdateret 24. marts 2022 Hvad er isomerer? Isomerer er forbindelser, der deler den samme molekylære formel, men adskiller sig i struktur eller rumlig arrangement. De falder i to hov
At tælle alkanisomerer:en praktisk vejledningAf Kevin Beck | Opdateret 24. marts 2022 Hvad er isomerer? Isomerer er forbindelser, der deler den samme molekylære formel, men adskiller sig i struktur eller rumlig arrangement. De falder i to hov -
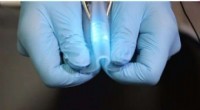 Sådan ser et stretchy kredsløb udForskere i Kina har lavet et nyt hybrid ledende materiale - del elastisk polymer, del flydende metal - der kan bøjes og strækkes efter ønske. Kredsløb lavet med dette materiale kan have de fleste todi
Sådan ser et stretchy kredsløb udForskere i Kina har lavet et nyt hybrid ledende materiale - del elastisk polymer, del flydende metal - der kan bøjes og strækkes efter ønske. Kredsløb lavet med dette materiale kan have de fleste todi -
 Gennembrud i sur vandelektrolyse via rutheniumbaserede katalysatorerIltudviklingsreaktion (OER) og oxygenreduktionsreaktion (ORR) kan betragtes som to trofæer inden for effektiv udnyttelse af brintenergi. Imidlertid, i sur OER, et stort anvendt potentiale var påkrævet
Gennembrud i sur vandelektrolyse via rutheniumbaserede katalysatorerIltudviklingsreaktion (OER) og oxygenreduktionsreaktion (ORR) kan betragtes som to trofæer inden for effektiv udnyttelse af brintenergi. Imidlertid, i sur OER, et stort anvendt potentiale var påkrævet -
 Kryo-elektronmikroskopi kaster nyt lys over batterierKredit:Kourkoutis Lab Grænsefladen mellem den faste anode og den flydende elektrolyt spiller en afgørende rolle i ydelsen af et lithium-metalbatteri, men karakterisering af de processer, der ske
Kryo-elektronmikroskopi kaster nyt lys over batterierKredit:Kourkoutis Lab Grænsefladen mellem den faste anode og den flydende elektrolyt spiller en afgørende rolle i ydelsen af et lithium-metalbatteri, men karakterisering af de processer, der ske
- Mørke fibre lægger grunden til jordskælvsdetektion over lange afstande og kortlægning af grundva…
- Hvad kaldes delene af et levende system?
- Hvordan forklarer begrebet et felt handling på afstand?
- Hvor mange AU er Merkur?
- Tight squeeze for Hong Kongs unge professionelle
- Interaktion mellem klimafaktorer og tidsskala påvirker vurderingen af ekstrem tørke i Kina


