Svovlsyre i nitrobenzensyntese:rolle og mekanisme
Sådan gør du:
1. Dehydrerende middel:
* Salpetersyre (HNO₃), den anden reaktant, er en svag elektrofil. For at øge dets elektrofilicitet skal det protoneres.
* Svovlsyre, som er en stærk syre, protonerer salpetersyre for at danne nitroniumionen (NO₂⁺), en stærk elektrofil.
*Reaktionen:
HNO₃ + H₂SO4 ⇌ H₂NO₃⁺ + HSO4⁻
H₂NO₃⁺ ⇌ NO₂⁺ + H₂O
2. Katalysator:
* Nitroniumionen angriber derefter benzenringen, hvilket fører til dannelsen af nitrobenzen.
*Reaktionen:
C₆H6 + NO₂⁺ → C₆H₅NO₂ + H⁺
* Svovlsyre hjælper også med at fjerne det vand, der produceres i reaktionen, og driver ligevægten hen imod dannelsen af nitrobenzen.
Sammenfattende er svovlsyrens nøgleroller i nitrobenzensyntesen:
* Protonerende salpetersyre for at danne nitroniumionen.
* Fungerer som en katalysator for at lette reaktionen.
* Fjernelse af vand for at flytte ligevægten mod produktdannelse.
Uden svovlsyre ville reaktionen forløbe meget langsomt, hvis overhovedet.
 Varme artikler
Varme artikler
-
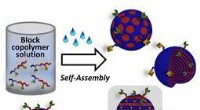 Oprettelse og selektiv funktionalisering af viruslignende polymerpartiklerSkematisk illustration af værket. Kredit:John Wiley &Sons, Inc. Forskere ved Tohoku University i Japan har samarbejdet med andre for at udvikle en enkel måde at skabe og funktionalisere virusligne
Oprettelse og selektiv funktionalisering af viruslignende polymerpartiklerSkematisk illustration af værket. Kredit:John Wiley &Sons, Inc. Forskere ved Tohoku University i Japan har samarbejdet med andre for at udvikle en enkel måde at skabe og funktionalisere virusligne -
 Nyt elektrodemateriale udviklet til at øge opladningskapaciteten af lithium-batterierNyt elektrodemateriale udviklet til at øge opladningskapaciteten af lithium-batterier. Kredit:Yokohama National University Lithium-batterier lover meget for fremtiden for mange applikationer, he
Nyt elektrodemateriale udviklet til at øge opladningskapaciteten af lithium-batterierNyt elektrodemateriale udviklet til at øge opladningskapaciteten af lithium-batterier. Kredit:Yokohama National University Lithium-batterier lover meget for fremtiden for mange applikationer, he -
 Nøjagtig bestemmelse af energiniveauerne for forskellige solceller til højtydende enhedera) Energiniveauer for organiske halvledere målt ved hjælp af UPS, LE-IPES og CV. b,c) Plot, der viser sammenhængen mellem Eoxd og IE (målt via UPS) (b), og Erød og EA (målt via LE-IPES) (c) af donorpo
Nøjagtig bestemmelse af energiniveauerne for forskellige solceller til højtydende enhedera) Energiniveauer for organiske halvledere målt ved hjælp af UPS, LE-IPES og CV. b,c) Plot, der viser sammenhængen mellem Eoxd og IE (målt via UPS) (b), og Erød og EA (målt via LE-IPES) (c) af donorpo -
 Sådan suger du kuldioxid fra himlen til brændstof og mereCarbon Engineerings rene brændstof, syntetiseret fra kuldioxid fanget fra luften og brint spaltet fra vand. Kredit:Carbon Engineering En skønne dag, den benzin, du køber, kan spore sin arv til kul
Sådan suger du kuldioxid fra himlen til brændstof og mereCarbon Engineerings rene brændstof, syntetiseret fra kuldioxid fanget fra luften og brint spaltet fra vand. Kredit:Carbon Engineering En skønne dag, den benzin, du køber, kan spore sin arv til kul


