Molekylær opløselighed:Opløses faste stoffer i individuelle molekyler i vand?
* Molekylære faste stoffer: Disse faste stoffer holdes sammen af svage intermolekylære kræfter (som hydrogenbinding, dipol-dipol-interaktioner eller London-dispersionskræfter).
* Vandets polaritet: Vand er et meget polært molekyle, hvilket betyder, at det har en positiv og negativ ende. Denne polaritet gør det muligt for den at interagere med og forstyrre de svage kræfter, der holder det molekylære faste stof sammen.
* Opløsningsproces: Når et molekylært fast stof placeres i vand, omgiver de polære vandmolekyler de opløste molekyler. Tiltrækningskræfterne mellem vandmolekylerne og de opløste molekyler er stærkere end de intermolekylære kræfter i det faste stof. Dette får de opløste molekyler til at bryde fra hinanden og blive omgivet af vandmolekyler og danner en opløsning.
Vigtig bemærkning: Nogle molekylære faste stoffer er ikke særlig opløselige i vand. Dette kan forekomme, hvis de intermolekylære kræfter i det faste stof er meget stærke, eller hvis det opløste molekyle er upolært og ikke kan interagere godt med vand.
 Varme artikler
Varme artikler
-
 Opbygning af selvtest til verdens mest almindelige infektionssygdomme - med papirForskere har udnyttet papirets egenskaber til at bygge hurtigere, billigere og mere bærbare enheder til påvisning af infektionssygdomme. Kredit:Purdue University foto/Rebecca Wilcox Da et hiv-udbr
Opbygning af selvtest til verdens mest almindelige infektionssygdomme - med papirForskere har udnyttet papirets egenskaber til at bygge hurtigere, billigere og mere bærbare enheder til påvisning af infektionssygdomme. Kredit:Purdue University foto/Rebecca Wilcox Da et hiv-udbr -
 Rad afsløringer:Fremtidige brændstofdesigns fra ædle metallerKredit:Fysisk kemi Kemisk fysik Forskere ved PNNL fjerner et svøb af mystik omkring adfærden af visse metalpartikler i nukleart brændsel. Holdets resultater kan forbedre fremtidige brændselsdesig
Rad afsløringer:Fremtidige brændstofdesigns fra ædle metallerKredit:Fysisk kemi Kemisk fysik Forskere ved PNNL fjerner et svøb af mystik omkring adfærden af visse metalpartikler i nukleart brændsel. Holdets resultater kan forbedre fremtidige brændselsdesig -
 Ny 3D-printteknik er en game changer for medicinske testenhederEt eksempel på en mikrofluidisk chip skabt af forskerholdet. Kredit:Yang Xu Mikrofluidiske enheder er kompakte testværktøjer, der består af bittesmå kanaler skåret på en chip, som gør det muligt fo
Ny 3D-printteknik er en game changer for medicinske testenhederEt eksempel på en mikrofluidisk chip skabt af forskerholdet. Kredit:Yang Xu Mikrofluidiske enheder er kompakte testværktøjer, der består af bittesmå kanaler skåret på en chip, som gør det muligt fo -
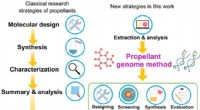 Design af højtydende hypergoliske drivmidler til rumraketter baseret på materialernes genomNy strategi i design af drivmiddel baseret på genommetoden. Kredit:Science Advances, doi:10.1126/sciadv.abb1899 En ny generation af raketdrivmidler til udforskning af det dybe rum, såsom ioniske f
Design af højtydende hypergoliske drivmidler til rumraketter baseret på materialernes genomNy strategi i design af drivmiddel baseret på genommetoden. Kredit:Science Advances, doi:10.1126/sciadv.abb1899 En ny generation af raketdrivmidler til udforskning af det dybe rum, såsom ioniske f
- Hvad er der nødvendigt for at overføre og frigive energi?
- Californiske brandmænd jagter nye brande antændt af lyn
- Materiale og belægningsproces for at beskytte keramiske dele
- Ren luft er en homogen blanding?
- Genomforskning udfordrer tidligere forståelse af fotosyntesens oprindelse
- STEM:Bestræbelser på at inspirere flere børn kunne forankre uddannelsesmæssige uligheder


