Metalreaktivitet i vandige opløsninger:reaktioner og opløsning
1. Ingen reaktion:
* Ædelmetaller: Nogle metaller, som guld og platin, er meget ureaktive og vil ikke reagere med de fleste almindelige vandige opløsninger.
* Ikke-reaktive løsninger: Hvis opløsningen blot er vand eller en ikke-reaktiv saltopløsning, kan metallet simpelthen sidde der og ikke reagere.
2. Opløsning:
* Reaktive metaller: Nogle metaller, som natrium og kalium, er meget reaktive og vil reagere kraftigt med vand, frigive brintgas og danne et metalhydroxid.
* Syreløsninger: Mange metaller vil reagere med sure opløsninger, frigive brintgas og danne et metalsalt. Reaktiviteten afhænger af metallet og syrestyrken.
* Oxiderende løsninger: Nogle metaller vil opløses i opløsninger, der indeholder stærke oxidationsmidler, såsom salpetersyre eller koncentreret svovlsyre. Metallet vil blive oxideret og danne metalioner i opløsning.
3. Forskydningsreaktioner:
* Flere reaktive metaller: Hvis et mere reaktivt metal anbringes i en opløsning, der indeholder en mindre reaktiv metalion, vil det mere reaktive metal fortrænge det mindre reaktive metal fra opløsning. For eksempel vil placering af jern (Fe) i en kobber(II)sulfatopløsning resultere i dannelsen af jern(II)sulfat og metallisk kobber. Dette følger reaktivitetsrækken af metaller.
4. Dannelse af et beskyttende lag:
* Aluminium og jern: Nogle metaller danner et tyndt oxidlag på deres overflade, når de udsættes for luft eller vand. Dette oxidlag kan være beskyttende og forhindre yderligere reaktion med opløsningen.
Faktorer, der påvirker reaktionen:
* Metalreaktivitet: Metallets reaktivitet bestemmer, hvor let det vil reagere med en opløsning.
* Løsningskoncentration: En højere koncentration af de reagerende arter i opløsningen vil generelt øge reaktionshastigheden.
* Temperatur: Forøgelse af temperaturen øger generelt reaktionshastigheden.
* Tilstedeværelse af katalysatorer: Nogle reaktioner kan katalyseres af tilstedeværelsen af visse stoffer.
Eksempler:
* Natrium (Na) i vand: Kraftig reaktion, der producerer hydrogengas og natriumhydroxid.
* Zink (Zn) i saltsyre (HCl): Reaktion producerer hydrogengas og zinkchlorid.
* Kobber (Cu) i sølvnitrat (AgNO3): Fortrængningsreaktion, der danner sølv(Ag)metal og kobber(II)nitrat.
Samlet set:
Interaktionen mellem et fast metal og en vandig opløsning er kompleks og kan føre til forskellige reaktioner afhængigt af det specifikke metal og opløsningen. Forståelse af reaktivitetsrækken af metaller og opløsningens egenskaber er afgørende for at forudsige resultatet af sådanne interaktioner.
 Varme artikler
Varme artikler
-
 Polymer lyser reversibelt hvidt, når det strækkesDen nyudviklede polymer tænder og slukker for sin fluorescens ved at reagere på mekanisk stress. Kredit:Hokkaido University Forskere ved University of Fribourgs Adolphe Merkle Institute (AMI) og H
Polymer lyser reversibelt hvidt, når det strækkesDen nyudviklede polymer tænder og slukker for sin fluorescens ved at reagere på mekanisk stress. Kredit:Hokkaido University Forskere ved University of Fribourgs Adolphe Merkle Institute (AMI) og H -
 Ny 3D-printproces tilbyder nye muligheder for energilagringsdesignForskere ved UNSW Sydney brugte en standard 3D-printer til at producere et indviklet kort over Australien lavet af fast polymerelektrolyt, som derefter blev testet som en energilagringsenhed. Kredit:D
Ny 3D-printproces tilbyder nye muligheder for energilagringsdesignForskere ved UNSW Sydney brugte en standard 3D-printer til at producere et indviklet kort over Australien lavet af fast polymerelektrolyt, som derefter blev testet som en energilagringsenhed. Kredit:D -
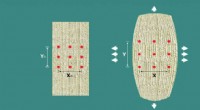 2D-materialer tilbyder unikke strækegenskaberAuxetiske materialer bliver tykkere, når de strækkes og tyndere, når de komprimeres. Det auxetiske materiale til venstre vokser i bredden, når det trækkes i lodret retning, som vist til højre. Kredit:
2D-materialer tilbyder unikke strækegenskaberAuxetiske materialer bliver tykkere, når de strækkes og tyndere, når de komprimeres. Det auxetiske materiale til venstre vokser i bredden, når det trækkes i lodret retning, som vist til højre. Kredit: -
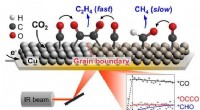 Kuldioxid omdannet til ethylen - industriens risRealtidsanalyse af katalytisk overflade i processen med elektrokemisk kuldioxidkonvertering af ethylen. Kredit:Korea Institute of Science and Technology (KIST) I den seneste tid, elektrokemisk kon
Kuldioxid omdannet til ethylen - industriens risRealtidsanalyse af katalytisk overflade i processen med elektrokemisk kuldioxidkonvertering af ethylen. Kredit:Korea Institute of Science and Technology (KIST) I den seneste tid, elektrokemisk kon
- Hvad er de grundlæggende enheder af Watt?
- Global gletsjersmeltning hæver havniveauet og udtømmer en gang pålidelig vandkilde
- Hvad er biologi-?
- 1. En note har en bølgelængde på 0,77955 m. Hvis hastighedslyden er 343,00 ms, hvilken tonehøjde…
- Hvornår lærte mennesker første gang at tælle?
- Hvordan reducerer man drivhusgasser? Tips fra en metanædende mikrobe


