Forståelse af metalfaste stoffer:struktur, binding og egenskaber
Her er en oversigt:
* Krystallinsk fast stof: Atomerne er arrangeret i et højt ordnet, gentagende mønster, hvilket skaber et krystalgitter.
* Metalbindinger: Valenselektronerne er delokaliserede, hvilket betyder, at de ikke er bundet til noget specifikt atom og kan bevæge sig frit gennem gitteret. Dette skaber et "hav af elektroner", der holder de positivt ladede metalioner sammen.
Her er nogle nøgleegenskaber, der er resultatet af disse egenskaber:
* Høj elektrisk ledningsevne: De frie elektroner kan nemt føre en elektrisk strøm.
* Høj varmeledningsevne: De frie elektroner kan overføre varmeenergi hurtigt.
* Smidbarhed og duktilitet: De metalliske bindinger gør det muligt for atomerne at glide forbi hinanden, hvilket gør metaller let formede.
* Lans: De delokaliserede elektroner reflekterer lys, hvilket giver metaller deres karakteristiske glans.
Opsummering: Metalfaste stoffer er unikke på grund af deres stærke metalliske bindinger, hvilket fører til en række vigtige egenskaber, der gør dem essentielle i forskellige applikationer.
Sidste artikelNatriumion (Na+) vs. Neonatom (Ne):Nøgleforskelle forklaret
Næste artikelEn historie om giftgas:oprindelse og udvikling
 Varme artikler
Varme artikler
-
 Ny bøjelig smartphone-teknologi kan bruge overvågning til at redde patienters livPurdue University-forskere arbejder på at bruge en ny polymerfilm, som kunne gøre smartphones mere bøjelige, at skabe skræddersyede sensorer, der ikke-invasivt kunne overvåge glukoseniveauer, hjertefr
Ny bøjelig smartphone-teknologi kan bruge overvågning til at redde patienters livPurdue University-forskere arbejder på at bruge en ny polymerfilm, som kunne gøre smartphones mere bøjelige, at skabe skræddersyede sensorer, der ikke-invasivt kunne overvåge glukoseniveauer, hjertefr -
 Forskere syntetiserer et materiale, der er i stand til at nedbryde nervestoffer i vandKredit:CC0 Public Domain Et team fra Institute of Molecular Science (ICMol) fra University of Valencia er lykkedes med at syntetisere et nyt porøst materiale, der muliggør og styrer nedbrydning af
Forskere syntetiserer et materiale, der er i stand til at nedbryde nervestoffer i vandKredit:CC0 Public Domain Et team fra Institute of Molecular Science (ICMol) fra University of Valencia er lykkedes med at syntetisere et nyt porøst materiale, der muliggør og styrer nedbrydning af -
 Tynde lag vand lover løfte om fremtidens energilagringLavtemperatur høj opløsning transmissionselektronmikroskop billede af en trombocyt af wolframoxiddihydrat; striberne er individuelle lag af atomer adskilt af vandlag. Kredit:North Carolina State Unive
Tynde lag vand lover løfte om fremtidens energilagringLavtemperatur høj opløsning transmissionselektronmikroskop billede af en trombocyt af wolframoxiddihydrat; striberne er individuelle lag af atomer adskilt af vandlag. Kredit:North Carolina State Unive -
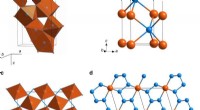 Forskere skaber umulige materialer på en enkel mådeKrystalstrukturer af jern-nitrogenforbindelser. Orange og blå kugler viser positionerne af Fe- og N -atomer, henholdsvis. (a) Fe3N2 ved 50? GPa. Strukturen er bygget af firkantede trigonale prismer NF
Forskere skaber umulige materialer på en enkel mådeKrystalstrukturer af jern-nitrogenforbindelser. Orange og blå kugler viser positionerne af Fe- og N -atomer, henholdsvis. (a) Fe3N2 ved 50? GPa. Strukturen er bygget af firkantede trigonale prismer NF
- Hybride Janus nanopartikler fremstillet af guld og titaniumoxid har høj katalytisk aktivitet og eks…
- Før energien i fødevarer kan bruges af en celle, der først skal overføres til molekyler af hvad?…
- Myrernes medicin:Redning og behandling af sårede personer
- Billede:Proba-1 billeder Calanda reservoir
- Hvad er et væv, der bevæger sig og næringsstoffer gennem plante?
- Gaia spionerer to midlertidigt forstørrede stjerner


